

心率(HR)升高是心血管疾病患者左心室重构、不良心血管结局以及更高全因死亡率的独立危险因素[1,2]。伊伐布雷定是一种新型的单纯降低窦性心率的药物,且对心脏电传导无影响,已用于治疗窦性心率大于70次/分的心绞痛或射血分数降低的心力衰竭(HFrEF)患者[3]。然而,从几项研究得出的结论来看,伊伐布雷定对慢性心衰患者再住院和心功能的影响仍不一致[4,5]。为此,重庆医科大学附属第一医院心血管内科团队(罗素新,Bryan Richard,黄毕等)于2022年4月在美国Clinical Cardiology杂志发表了一项荟萃分析[6],旨在阐明伊伐布雷定对慢性HFrEF患者的疗效。
联合伊伐布雷定可显著降低HFrEF患者心率,改善LVEF和运动能力
研究团队筛选出联合应用伊伐布雷定的6项随机对照试验和1项亚组分析,包括7074例患者(安慰剂组3523例,伊伐布雷定组3551例),进行了本项荟萃分析。
荟萃分析结果表明,与安慰剂组相比,在标准心衰治疗基础上加用伊伐布雷定可降低静息心率约10次/分;使LVEF增加约3.89%(图1);并提高运动耐力,使运动持续时间增加约8.52分钟。运动能力的提高得益于β-受体阻滞剂与伊伐布雷定的联合应用,增加了β-受体阻滞剂对α-肾上腺素能受体的非选择性作用,从而影响运动时骨骼肌的扩张[7]。此外,伊伐布雷定已被证明可以维持运动引起的血管扩张,增加运动时的肌肉血流量,并改善外周血流量[7]。
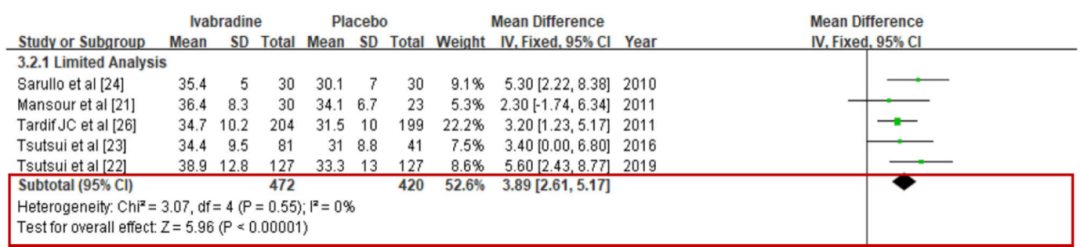
图1 伊伐布雷定与安慰剂比较,对LVEF的影响
伊伐布雷定可显著改善左心室重构相关指标及可能机制
3项慢性HFrEF的超声心动图试验(安慰剂组252例,伊伐布雷定组264例)被纳入观察伊伐布雷定对左心室重构的影响。结果显示,在标准心衰治疗的基础上加用伊伐布雷定可显著缩小左心室收缩末期内径(-3.73;95%CI -4.25, -3.21)、舒张末期内径(-1.43;95%CI -2.78, -0.08 )、左心室收缩末期容积(-17.00;95%CI -29.65, -4.35)。
一些研究猜测伊伐布雷定改善心脏重构的潜在机制是改善心肌细胞功能,优化能量消耗,改善内皮功能,逆转电生理变化,减少RAAS刺激和交感兴奋等[8]。此外,超极化激活的环核苷酸门控(HCN)通道在窦房结细胞外其他心肌细胞中的表达和功能,在心脏重构中的作用也逐渐被人们所认识。
一项动物研究[9]发现,心肌If升高调节钙离子稳态并导致不利的心脏重构。If增强导致舒张期Na+内流,从而使Na+/Ca2+交换平衡向反向模式移动,导致细胞内Ca2+浓度升高。细胞质内Ca2+稳态改变刺激细胞凋亡并且导致心室重构的发生(图2)。If的药理抑制(伊伐布雷定)可阻止细胞内Ca2+浓度升高,保护心室重塑。
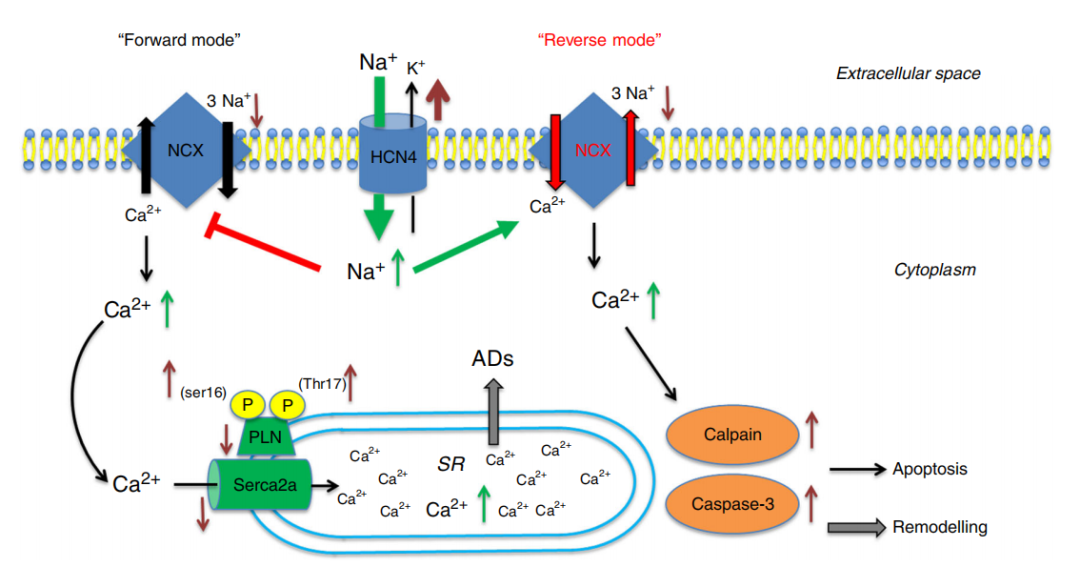
图2 心肌中HCN4表达增强可能导致病理重构的模型。HCN4表达上调介导舒张期Na+内流增多,使细胞内Na+增加;心肌细胞的Ca2+稳态与Na+以及NCX的调节紧密相关。在生理情况下,NCX主要以Na+入/ Ca2+出模式(Forward mode,正向模式)进行,从而降低舒张期细胞内Ca2+浓度。HCN4表达上调使细胞内Na+浓度增加,进而使NCX调节向反向模式(Reverse mode)进行,从而导致细胞内Ca2+浓度增加。细胞质内Ca2+循环的改变干扰了SR中Ca2+的吸收,SR中Ca2+的超载导致ADs和心律失常;而且,舒张期胞浆内高Ca2+浓度会激活细胞凋亡的关键酶Calpain和caspase-3, 导致心室重构的发生。NCX:钠钙交换体;HCN4:超极化激活的环核苷酸门控通道(HCN),HCN4为其中一亚型;ADs:afterdepolarizations,后去极化;PLN:phospholamban,磷化氢;SR:sarcoplasmic reticulum ,肌浆网;Serca2a:肌浆网钙泵;Calpain:钙依赖蛋白酶;Caspase-3:半胱氨酸天冬氨酸蛋白酶-3;棕色箭头表示蛋白表达调控;绿色箭头表示离子浓度的变化。
伊伐布雷定可显著降低因心衰恶化再入院
该项荟萃分析显示,伊伐布雷定治疗后因心衰恶化再入院的发生率显著降低(RR=0.76;95%CI 0.69,0.84),而心血管死亡率无统计学差异(RR=0.92;95%CI 0.82,1.03)。伊伐布雷定组视觉障碍和无症状心动过缓事件显著增加。
总结
该项荟萃分析表明,除了上述几种不良事件(无症状心动过缓和视觉障碍)外,伊伐布雷定治疗不仅安全,而且对慢性HFrEF患者的心率降低、心功能改善和更好的运动耐量都是有益的。这项荟萃分析也是为数不多的讨论伊伐布雷定对慢性HFrEF患者影响的荟萃分析之一。
参考文献
[1] Kannel WB, Kannel C, Paffenbarger RS Jr, et al. Heart rate and cardiovascular mortality: the Framingham study. Am Heart J. 1987;113(6):1489-1494. https://doi.org/10.1016/0002-8703(87)90666-1.
[2] Fox K, Borer JS, Camm AJ, et al. Resting heart rate in cardiovascular disease. J Am Coll Cardiol. 2007;50(9):823-830. https://doi.org/10.1016/j.jacc.2007.04.079.
[3] Task Force Members, Montalescot G, Sechtem U, et al. 2013 ESC guidelines on the management of stable coronary artery disease: the Task Force on the management of stable coronary artery disease of the European Society of Cardiology. Eur Heart J. 2013;34(38):2949-3003. https://doi.org/10.1093/eurheartj/eht296.
[4] Fox K, Ford I, Steg PG, Tendera M, Ferrari R. Ivabradine for patients with stable coronary artery disease and left-ventricular systolic dysfunction(BEAUTIFUL): a randomised, double-blind, placebocontrolled trial. Lancet. 2008;372(9641):807-816. https://doi.org/10.1016/S0140-6736(08)61170-8.
[5] Sarullo FM, Fazio G, Puccio D, et al. Impact of “off-label” use of ivabradine on exercise capacity, gas exchange, functional class, quality of life, and neurohormonal modulation in patients with ischemic.chronic heart failure. J Cardiovasc Pharmacol Ther. 2010;15(4):349-355. https://doi.org/10.1177/1074248410370326.
[6] Richard SB, Huang B ,Liu G, Yang Y, Luo SX, et al. Impact of ivabradine on the cardiac function of chronic heart failure reduced ejection fraction: Meta-analysis of randomized controlled trials. Clin Cardiol. 2021 Apr;44(4):463-471.doi: 10.1002/clc.23581. Epub 2021 Feb 27.
[7] Simon L, Ghaleh B, Puybasset L, et al. Coronary and hemodynamic effects of S 16257, a new bradycardic agent, in resting and exercising conscious dogs. J Pharmacol Exp Ther. 1995;275(2):659-666.
[8] Vercauteren M, Favre J, Mulder P, et al. Protection of endothelial function by long term heart rate reduction induced by ivabradine in a rat model of chronic heart failure. Fundam Clin Pharmacol. 2007;21:22-22.
[9] Yampolsky P, et al. Augmentation of myocardial If dysregulates calcium homeostasis and causes adverse cardiac remodeling. Nat Commun. 2019 Jul 23;10(1):3295. doi: 10.1038/s41467-019-11261-2.

罗素新,重庆医科大学附属第一医院心血管内科主任;教授、主任医师、医学博士、博士生导师、留美学者;重庆英才·创新领军人才(医学领域);重庆市学术技术带头人(心血管内科);全三八”红旗手标兵;重医附一院"学习钱悳精神"好医生;中国胸痛中心、心衰中心和心脏康复中心评审专家和执委会委员;中华医学会内科学专委会常委;中国医师协会心力衰竭国“五一”巾帼标兵;重庆市“五一”劳动奖章;主持国家自然科学基金面上项目2项和省部级课题14项;主编临床医学教材1部、发表论文90余篇、SCI 40余篇;擅长冠心病、心力衰竭等疾病的诊治及起搏器和冠脉介入诊疗技术。