


本文综合国内外文献,全面阐述了衰竭心脏能量代谢药物治疗新动向,强调各种原因引发的心力衰竭,心肌缺血,心肌肥厚,心肌梗死,缺血性脑卒中,脑外伤,脑昏迷,帕金森病,药物诱发的心肌病,婴幼儿心肌炎等等心脑血管病,都有程度不同的能量代谢异常。21世纪医学的发展认为:衰竭心脏是一台缺乏燃料的引擎(failing heart is an engine out of fuel),据此,明确提出了能量代谢调控是治疗慢性心衰的新靶点!而磷酸肌酸就是治疗慢性心衰新靶点的基石药物。为此,笔者认为,临床必需转变观念: 磷酸肌酸既不是一般的营养药,更不是什么辅助用药,而是名正言顺的治疗用处方药!
众所周知,心脏平均每天搏动10万次,每搏输出60~80ml血液,即每天向全身输送6~8吨血液。心脏的收缩与舒张是一个主动耗能过程,ATP是心肌唯一可利用的能源形式。人体每天约消耗43kgATP,其中心脏搏动消耗6kg,即每秒消耗1mmolATP,(0.507g)。>90%ATP是源自心肌线粒体的磷酸肌酸(Creatine Phosphate,CrP),然而,心脏很小, 如此大量的ATP是无法储存备用的,仅约有20mmol Pi (ATP和CrP的高能磷酸键); 合成后的ATP也必须在短时间内消耗 。巧夺天工的心脏,又是一个高效率的能量生成、供给器官, 依靠每天每个ATP分子重复利用1000-1500次,即能满足每天6kgATP的能量需要, 而CrP则扮演了如此穿梭运动中的主角—梭子:由葡萄糖和游离脂肪酸经氧化反应生成ADP,继之,ADP依靠CrP形成ATP,再从ATP释放出能量(Pi,高能磷酸键,为心肌利用)后变成ADP,ADP再依靠CrP形成ATP,如此穿梭循环不已,满足了心脏搏动的能量需要[1~3]。
肌酸(Cr)广泛存在于自然界的动植物中。人体各种细胞均有,>95%是在肌肉。其中1/3为游离Cr,2/3为CrP,此比例随人种、年龄、疾病等因素而改变。首次发现Cr是动植物的重要组成成分的是1832 年法国化学家Michel Chevreul,从而奠定了肌肉代谢机制―中心法则的科学基础;1847年认识到Cr在肌肉工作的生理作用;1911年又发现Cr在肌肉代谢的机制;1930年了解到CrP是肌肉收缩的主要能源,每摩尔供能12000卡,远高于ATP 7300卡或ADP380卡;1939年又认识到CrP的合成与氧耗偶联,证明在肌肉中,Cr的氧化磷酰化反应至关重要!迟至1960年方启动ATP与CrP的生物合成;1970年发现CrP可提高工作能中,从1990年开始广泛将CrP用于运动员,尤其是足球、摔跤、曲棍球以及体操运动员!进入21世纪,CrP已发展成为治疗慢性心衰新靶点的基石药物[1,2]。
内源性Cr是由精氨酸与甘氨酸在精氨酸-甘氨酸氨基转移酶(AGAT)催化下形成胍基乙酸(GAA),再在胍基乙酸-N-甲基转移酶(GAMT)催化下,由S-腺苷甲硫氨基酸供给甲基不可逆地形成Cr,最后经肌酸激酶作用经磷酰化生成CrP。控制CrP生成的三种机制:一是细胞内外CrP浓度反馈性调节AGAT的活性;二是Cr转运蛋白的活性和三是某些介质或激素增加对Cr的净摄取,如异丙肾上腺素,去甲肾上腺素,胰岛素(超剂量)以及胰岛素样生长因子。内源性Cr的合成主要在肾脏和肝脏,每天约合成2.0g,由血液转运至肌肉,心脏,脑等处。外源性Cr主要由食物摄入, 每天约为1.0g。人体大约每天有1.5%~2%肌酸转化为肌酐由尿排出。一个70kg的健康男性,体内有120g总Cr池,当肌肉池内的Cr低于阈值时,即启动摄取过程[1,2]。
心力衰竭是一个艰巨的医学难题,也是造成社会的沉重负担。在英国约消耗GDP的2%;而在美国,每年为此而消耗280亿美金!更有甚者,在未来的10年,随着人口的老龄化,该病的财政支出将越加沉重[3]。
慢性心力衰竭也是一种常见病,占全美人口的2%以上,约有500万,在明确诊断后的一年内,有30%~40%的患者将会死亡。心力衰竭是所有心血管疾病的最终阶段,不仅使人致残,更严重的是影响生活质量[3]。
在过去的20年,对慢性心力衰竭的治疗获得了巨大进展,诸如血管紧张素转换酶抑制剂;ACEI)、醛固酮拮抗剂、β受体拮抗剂、血管紧张素受体拮抗剂(ARB)以及心脏复苏术等的应用。然而,即使采纳了现代化的治疗, 慢性心衰仍然有高达10%的死亡率!因此,研究更好的防治方法,是当前对心脏病学的一个重大挑战[3]!
慢性心力衰竭是多因素所致。包括神经体液系统,基因调控,炎症反应以及能量代谢失衡等。早在1939年,Herrmann 和Decherd两位教授即提出能量饥饿学说(The Energy-Starvation Hypothesis)[4]。之后,更多学者关注心肌功能与能量代谢之间的关系。如得克萨斯州卫生科学中心的Taegtmeyer教授,于2004年发表《心脏代谢机制应是衰竭心脏治疗的靶点》的重要文章。文章开宗明义、深有感触地指出: “生活中,没有几件事情比勿略显而易见的事情更为脑恨。一个典型例子是,早就应该把改善心肌能量底物代谢作为药物治疗心力衰竭的潜在靶点,而血流动力学的复杂性,冠脉血流以及心脏结构的研讨等,掩盖了这一简单的事实—心脏是一个高效的能量转换器”[5]。又如美国杰出心脏病学专家Braunwald也曾明确指出:“心力衰竭是一种被忽视的心肌能量饥饿,而能量饥饿又与心肌重构密切相关,三者呈恶性循环”[6]。
Katz教授对于慢性心力衰竭疾病的本质认识,作了最精辟的剖析:“心脏有如一匹虚弱且又疲惫的马,若能给予其足够的营养,便可恢复其精力并长时间工作,即使工作水平有所降低[7]。
时至今日,已有充分证据认为,衰竭心脏是一台缺乏燃料的引擎(failing heart is an engine out of fuel),这一观点极为重要,它明确提出了能量代谢调控是治疗慢性心衰的新靶点! 为今后20年慢性心力衰竭的防治指明了方向[3]。
体内供能的中心法则就是CrP+ ADP+H+ ⇄ATP+Cr,故CrP/ATP的比值是否正常(2.0~2.2)至关重要[8]。实验和临床均已证明,当心衰或心肌肥大时,比值显著下降,如冠心病、缺血性心肌梗死以及扩张性心肌病等,比值显著下降40%~70%。大量循证表明,当CrP/ATP比值>1.60时,心血管的死亡率为5%,总死亡率为10%,P值分别为0.016;0.036; 当CrP/ATP比值<1.60时, 心血管与总死亡率均高达40%。因此,在预测心衰致死的诸多风险因素中, CrP/ATP比值已成为一有意义的、独立的指标,并且提示,CrP/ATP 比值较以往预测心衰风险高低的左心室射血分数(LVEF)、脑鈉肽水平(Brain Natriuretic Peptides,BNP)以及传统的纽约心脏协会分级( NYHA)更为准确,惜目前实际操作、测算难度较大而仍停留在理论阶段[8]。当心力衰竭或心肌缺血时,CrP水平下降比ATP更多、更明显,所以,及时补充CrP,恢复正常的CrP/ATP比值是重中之重!
既然心脏不仅是一个泵,而且还是一个必需通过代谢获得大量能量的器官。代谢性疾病—心肌缺血,必需要用理想的、改善代谢的药物, 从短期血流动力学与药理学治疗,转变为长期心肌代谢的修复治疗。心力衰竭的用药原则由治疗为主转变为预防为主,即在以往的强心、利尿、扩血管的“金三角” 治疗原则基础之上,注入修复心肌储备能力的能量生成、转运和利用的新“三维模式”。为此,人类探索了近一个世纪, 从上世纪20年代研发的三磷腺苷(ATP)等腺苷类药物,到60年代的辅酶Q10、极化液,再到70年代的1,6二磷酸果糖、磷酸肌酸钠、哌克昔林(Perhexiline)以及曲美他嗪等,进而到90年代的左卡尼丁与多种氨基酸的应用,直到本世纪初雷诺嗪(Ranolazine),伊伐布雷定(Ivabradine)的问市等。大大丰富了该领域的理论与实践,更给患者带来了厚重的实惠。
直接供能是新三维模式中的支撑点,也是治疗慢性心衰新靶点的基石。心肌能量代谢药物治疗的突出特点,应是在不改变心率、血压或冠脉血流的前提下,通过直接供能;或不影响细胞完整性即改善心肌代谢机制,保障或提升心脏功能。总之,原则是不增加能量消耗或氧耗即可达到防治心衰的目的。迄今,只有CrP符合此要求,因为它是唯一可供临床药用的、直接供给高能量的内源性物质。此药与上述多种影响心肌能量代谢的药物相比, 无疑是疗效更高,安全性也更好!
众所周知,从认识CrP到实际批量生产、应用,几乎经历了半个世纪,因为CrP分子中有一极不稳定的高能磷酸键,在温度较高或有某些杂质存在时即可断裂而失效。为此,整个生产条件和工艺要求十分严格,必须保证产品是含有四个结晶水的针状结晶化合物,才符合稳定的质量标准。临床用其冻干粉针剂。磷酸肌酸四水二钠盐(Creatine phosphate disodium salt tetrahydrate),系白色针状结晶性粉末,由意大利阿尔法·韦士曼(ALFA WASSERMANN)制药厂在全球第一个率先合成、生产药用的CrP。磷酸肌酸的化学名:N-[亚氨基(膦氨基)甲基]-N-甲基甘氨酸二钠盐(N-[Imino(phosphonoamino)methyl]-N-methylglycine disodium salt),分子量为327.153,分子结构式(图1):
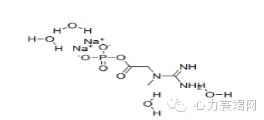
图1.Creatine phosphate disodium salt tetrahydrate
第一个研究证实CrP具有心脏保护作用的是,1970年Parratt与Marshall用豚鼠心肌制备急性缺血模型,给予CrP后,可使缺氧状态下的心肌收缩力增加>60%[8],其它多个试验也证明CrP具有显著的抗心律失常作用和保护心肌细胞肌膜以及缩小心肌坏死面积的作用。直至2005年,实验证实静脉注射本品亦同样获得显著改善心肌血流动力学,提高LVEF的效果。证明CrP具有心脏保护作用的另一经典实验是在心脏手术时的应用,即在传统冷冻化学心脏停搏液(Cardioplegic solution)中加入适量CrP(如10mmol/L,多次),可大大延长缺血性心脏骤停时间,并促进主动脉血流和心搏出量等术后缺血心肌功能的恢复,明显降低心血管事件[8]。
CrP的心脏保护作用的机制主要源自两个方面:一是通过区室化(compartmentalized)肌酸激酶(CK)反应,维持细胞局部ATP池, 即直接为心肌提供生物能源储备; 二是通过抗氧化—自由基,减少磷脂的流动性而稳定细胞膜, 细胞膜完整性的增强即可减少心肌坏死面积和心律失常的发生。因CrP为两性分子(Zwitterionic molecule),分子中N原子的正电荷与磷酸根的负电荷,在膜表面细胞分裂间期(interphase),与细胞膜磷脂分子中的正负电荷反向结合,阻滞或延缓膜磷脂降解为溶血磷脂甘油(Lysophosphoglycerides,LPG)。正是心肌一缺血区LPG的积聚,引发缺血心肌的电不稳定而致心律失常。CrP阻滞或延缓LPG的降解和抗脂质过氧化作用,使肌膜表面分裂间期的移动域(液相)转变为结构域(凝胶相),从而极大的增强细胞膜的稳定性。此外,参与生物能磷酸源储备的还有腺苷酸激酶(Adenylate kinase;AK)反应系统,AK催化2个分子ADP生成ATP、AMP各一分子,CrP还可抑制心肌细胞肌膜的5'核苷酶(5'-nucleotidase), 阻滞腺嘌呤核苷的降解,从而稳定细胞膜[8]。
FDA批准CrP的适应证,是心脏手术时加入心脏停搏液中以保护心肌,改善缺血状态下的心肌代谢异常。
首次将CrP用于心脏手术是1987年。心脏停搏液或晶体液中加与不加CrP的疗效差异显著,治疗组与对照组相比,显著缩短围手术期的心肌活动恢复时间,减少心电图异常、需除颤的瓦特功率与直流电休克数、心律失常(尤其是严重房室传导阻滞)以及正性肌力药物的用量和疗程等[8]。
CrP在心力衰竭的应用与研究十分广泛。仅在意大利超过1000例的多中心、对照研究就有两个:
1989年Grazioli等,主持49个临床心脏中心、共1,174例接受传统金三角治疗的心力衰竭患者,其中739例加用CrP2g/d,i.v.疗程3周;435例为对照组。结果,CrP治疗组心力衰竭的临床症状,如呼吸困难,肺充血,周围水肿以及缺血指征,如心绞痛,甘油三酯用量,T波倒置等均得到明显改善[9]。
1992年Grazioli等又开展一项多中心研究,58个临床心脏中心、共1007例NYHA Ⅲ、Ⅳ级的心力衰竭患者,其中,508例给予CrP i.v. 1g/bid,两周后改用肌内注射500mg/bid,四周。结果,NYHA Ⅲ、Ⅳ级的患者明显减少,尤其是静注的两周效果极佳,17%:26%,P<0.001;45天的疗效仍在9%:24%,P<0.001; 所有缺血指征,如心绞痛,甘油三酯用量,T波倒置,室性心律失常等均获得明显改善[10]。
近期,有三篇文献分别研究了CrP作为心肌保护药在急性冠脉综合征(ACS)、ACS后经皮冠脉介入治疗(PCI)或冠脉旁路搭桥术(CABG)中的应用。
Yang等报告[11]180例ACS后行PCI患者,男女兼有,平均63.6岁,随机均分两组:一组术后按常规治疗,另一组术后常规治疗外,即给予CrP 静点5天。观查指标是检测术前术后反映心肌损伤的酶谱:血清中肌酸激酶同工酶(CK-MB), 乳酸脱氢酶(LDH), 心肌肌鈣蛋白T(cTnT),超氧化物歧化酶( SOD),丙二醛(MDA )以及一氧化氮( NO)水平。结果, 加给CrP组, 术前术后与对照组相比,SOD显著增加;MDA、LDH、CK-MB显著降低;NO、cTnT则无统计学差异,结论是CrP对ACS后行PCI患者确有心肌保护作用。
Guo-Han C等报告[12]24例 (平均>65岁)施行CABG的老年患者,隨机均分两组:对照组给予心脏停搏液, 实验组给予心脏停搏液加CrP。在不同时间阻断主动脉并测定反映心肌损伤的酶谱。结果,两组MDA均有所增加,但对照组增加更为明显,P<0.01; 两组SOD有所下降,但实验组下降更为明显,P<0.01; 两组CK、CK-MB、LDH、cTnT均有所下降,但实验组下降更为明显,P<0.01。另电子显微镜观察线粒体的损伤,实验组的组织学变化更佳。作者结论为:国人行CABG的老年患者, 在心脏停搏液中加入CrP,不仅能为心肌细胞提供能量,而且还能缓解心肌缺血的再灌注和损伤。
Ke-Wu D等报告[13]400例ACS后行PCI患者,男女兼有 ,随机均分为两组:对照组PCI后按常规治疗;实验组术后常规治疗外,加给静点CrP3天,检测术前术后两组血清CK-MB与cTnT水平。结果,与对照组相比, 实验组8%的患者术后血清CK-MB增加1~3倍:5%的患者增加>3倍; 而对照组则分别降低19%和9%; 实验组12%的患者术后血清cTnT增加1~3倍:10%增加>3倍,而对照组则显著降低,分别为21%和18%。作者结论为:外源性CrP确能减轻PCI患者的心肌损伤。
林文辉等对CrP在药源性心脏病的保护作用进行了研究与报告[14]。共纳入120例恶性肿瘤患者,随机分为治疗组(60例)和对照组(60例),两组均采用含阿霉素类方案化疗,3~4周为1个疗程,共3个疗程,但治疗组在化疗的同时给予注射用磷酸肌酸钠1.0+0.9%氯化鈉100 mL,连用8~14 d。化疗3个疗程后评价疗效和心脏毒性。结果,治疗组和对照组的瘤体稳定率分别为76.67%和71.67%,差异无统计学意义(P=0.05)。治疗组和对照组的治疗前生活质量比较差异无统计学意义(P0.05);治疗后治疗组生活质量改善情况好于对照组(P=0.05)。治疗组的心电图改变发生率(41.67%)低于对照组(61.67%)(P=0.05);治疗组心肌缺血、心律失常和心肌酶异常发生率分别为45.00%、11.67%、10.00%,低于对照组的75.00%、41.67%、71.67%,差异均有统计学意义(P=0.01)。结论是注射用磷酸肌酸钠能够降低含阿霉素类方案所致心脏毒性的发生率,改善化疗患者的生活质量。此项研究提示,CrP不仅可预防蒽环类抗癌药的心脏毒,对其他具有心脏毒的药物或心脏损伤都有良好的防治作用。
CrP是唯一内源性供能药物,与其他用于能量代谢药物如三磷酸腺苷(ATP),1.6二磷酸果糖,药卡尼丁,曲美他嗪等相比,无疑具有极大的先天优势,CrP无需耗氧直接供能,且按分子比所含能量也最高。此外,CrP即刻生效非常适用于重危急症,而1.6二磷酸果糖与左卡尼丁是经氧化反应糖酵解供给能量, 曲美他嗪则是经氧化反应脂酵解供给能量,不仅需凭籍体内有限的氧(在心衰或心肌缺血时),且所产能量也较少。因为CrP是内源性物质,安全性也必然是最高,使用不受年龄、性别的限制,通常每天给予5g,疗程2个月, 临床几乎未见任何不良反应,只在剂量过大或滴注过快时,可见血压降低及钙的丢失等反应。
根据临床用药目的与病情进行个体化治疗。一般在心脏手术加在停搏液中的浓度为10mmol/L停搏液,相当于2.5g里尔统/升。如用于急性心梗和急性缺血性心脏疾病急性发作,可在 3-6h以内给予2-4g静脉滴注冲击给药,随之8-10g/d连续或分段静脉点滴,连续5天。如用于慢性缺血性心脏疾病,心脏衰竭(慢性心脏病或缺血心梗,扩张性心脏病或高血压性心脏病),在发作期5-10g/d,连用3-5d;发作期之后,1-2g/d,疗程2-6周。
值得注意的是,国家食品药品监督总局(CFDA)于2014年9月4日发出关注曲美他嗪可引起运动障碍等风险的警告[15],要求患有帕金森病、帕金森综合征、震颤、不安腿综合征以及其他相关的运动障碍者和严重肾功能损害的患者(肌酐清除率<30 ml/min)禁止使用曲美他嗪;中度肾功能损害的患者(肌酐清除率30-60 ml/min)和老年患者用药剂量也需适度调整。此外,建议曲美他嗪仅用于对一线抗心绞痛疗法控制不佳或无法耐受的稳定型心绞痛患者的对症治疗,不再用于耳鸣、眩晕的治疗。
总之,缺血状态下的心肌代谢异常,几乎涉及临床各个科室和多种疾病,诸如各种原因引发的心力衰竭,心肌缺血,心肌肥厚,心肌梗死,缺血性脑卒中,脑外伤,脑昏迷,帕金森病,药物诱发的心肌病,婴幼儿心肌炎等等心脑血管病,都有程度不同的能量代谢异常,均应及时补充CrP。为此,笔者认为,临床必需转变观念:CrP既不是一般的营养药,更不是什么辅助用药,而是名正言顺的治疗用处方药!
参考文献
1.Balsom PD, Söderlund K, Ekblom B. Creatine in humans with special reference to creatin supplementation Sports Med. 1994 Oct;18(4):268-80.
2.Bessman, SP Carpenter, CL。 The Creatine-Creatine Phosphate Energ Shuttle Annual Review of Biochemistry1985;54: 831-862
3.Stefan Neubauer. The Failing Heart — An Engine Out of Fuel N Engl J Med 2007;356:1140-51.
4. Herrmann G,Decherd GH.The chemical nature of heart failure Ann Intern Med 1939;12:1213~1214
5.Heinrich Taegtmeyer. Cardiac Metabolism as a Target for the Treatment of Heart Failure Circulation. 2004; 110: 894-896
6,Braunwald's .Heart Disease: Textbook Cardiovascular Medicine,Eighth Edition
7.Katz AM. Heart failure: pathophysiology,molecular biology and clinica management. Philadelphia: Lippincott Williams & Wilkins, 2000.
8. Strumia E,Pelliccia F,D'Ambrosio G. Creatine phosphate:Pharmacological and Clinical Perpectives Adv Ther 2012;29:99~123
9.Kley RA, Tarnopolsky MA, Vorgerd M.Creatine for treating muscle disorders Main results: CochraneLibrary 5 June 2013
9. Grazioli I, Strumia E.Terapia con creatina fosfato nel paziente con insufficienza cardiaca in fase di scompenso: Studio policentrico. G Ital Ric Clin Ter. 1989;10:39–45.
10.Grazioli I, Melzi G, Strumia E. Multicenter controlled study of creatine phosphate in the treatment of heart failure Curr Ther Res 1992;52: 271~280
11.JY Yang,JB Gong,LJ Wang.etal.Creatine phosphate protects the myocardium of acute coronary syndrome patients after percutaneous coronary intervention Journal of Medical Postgraduates;2012.03
12. Guo-Han C, Jian Hua G, Xuan H.etal.Role of creatine phosphate as a myoprotective agent during coronary artery bypass graft in elderly patients Coronary Artery Disease 2013, 24(1):48-53
13. Ke-Wu D, Xu-Bo S, Ying-Xin Z etal. The Effect of Exogenous Creatine Phosphate on Myocardial Injury After Percutaneous Coronary Intervention ANGIOLOGY 2015;66: 163-168
14. 林文辉 林雪华 谢彬. 注射用磷酸肌酸钠对阿霉素心脏毒性的保护作用
肿瘤基础与临床》 2010年01期
15. 国家食品药品监督管理总局. 限制曲美他嗪适应症并警惕其引起的运动障碍等安全性风险药品不良反应信息通报(第62期)2014年9月4日