

✦ 肿瘤心脏病学(Cardio-oncology)——应运而生,与时俱进
癌症患者长期生存率明显增加
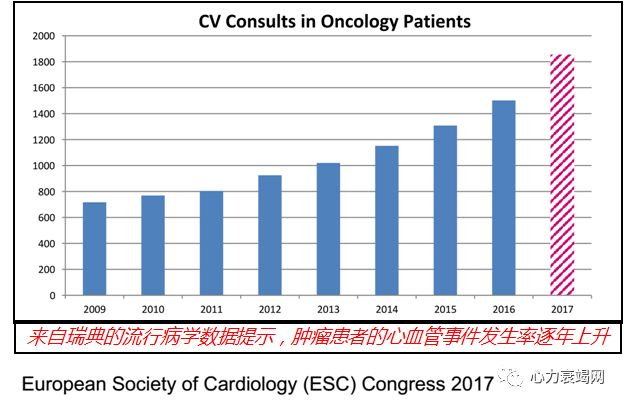
肿瘤治疗相关心血管不良反应发生率及致死率与日俱增
心血管疾病目前已成为癌症生存者的第二大死亡原因
抗肿瘤治疗不断推陈出新衍生越来越多的新兴临床问题
循证依据缺乏,临床处理存在困惑,诸多未知尚待探索



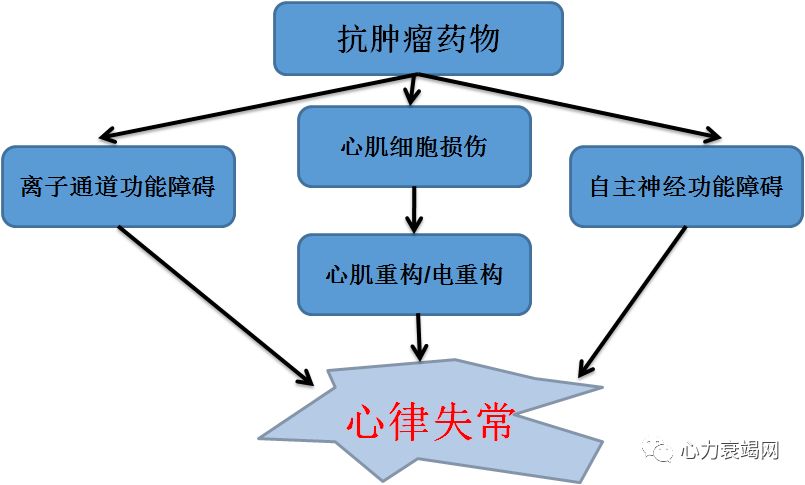
常见心律失常——
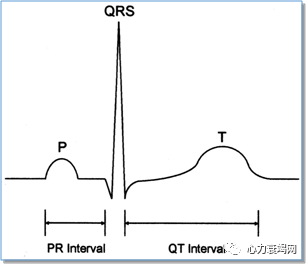
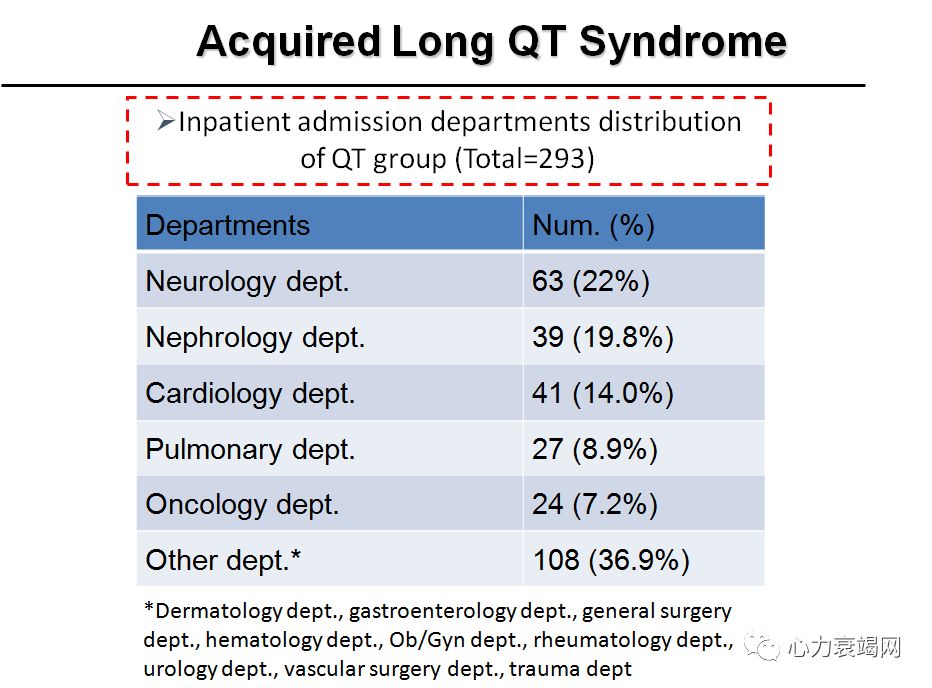
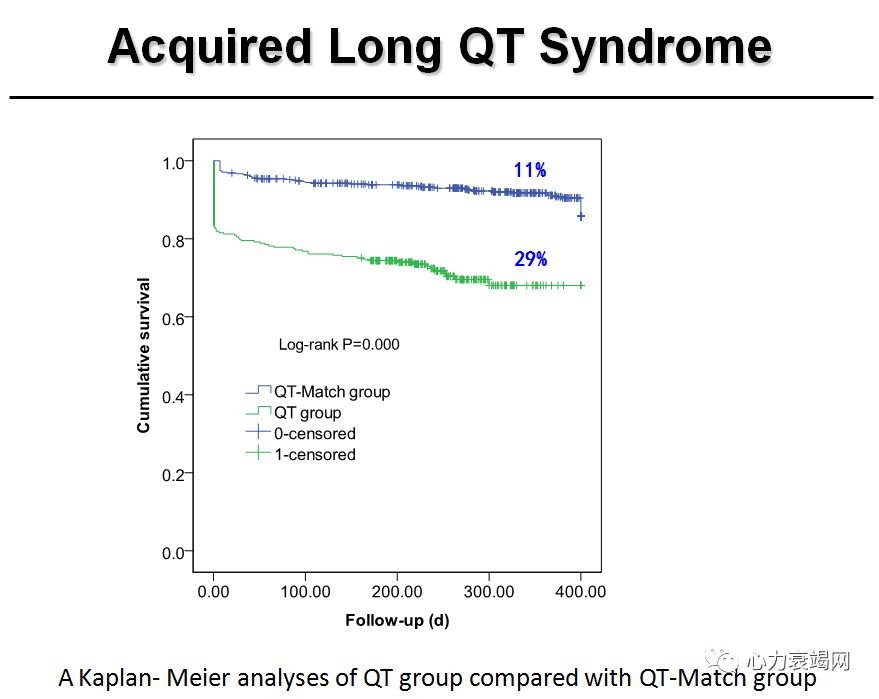
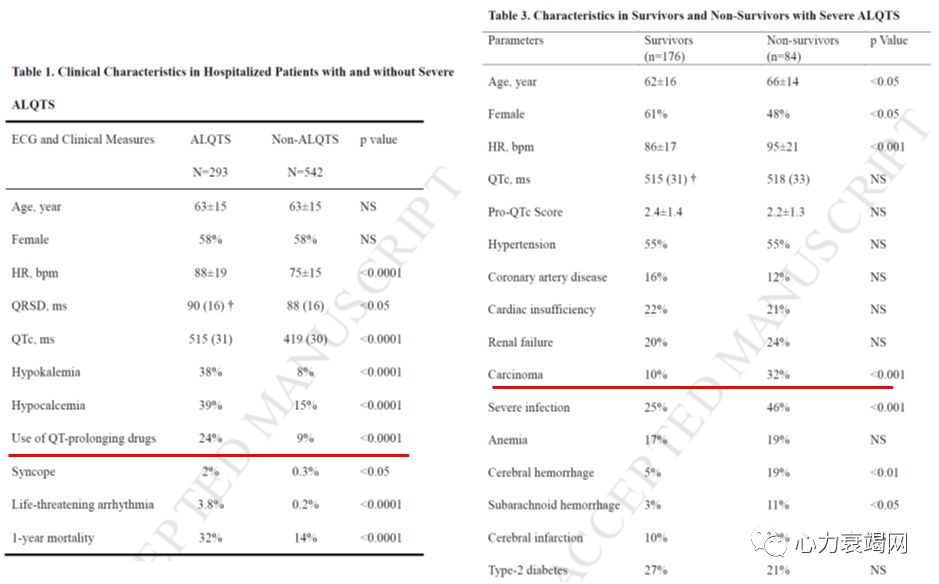
QT间期延长和尖端扭转型室速
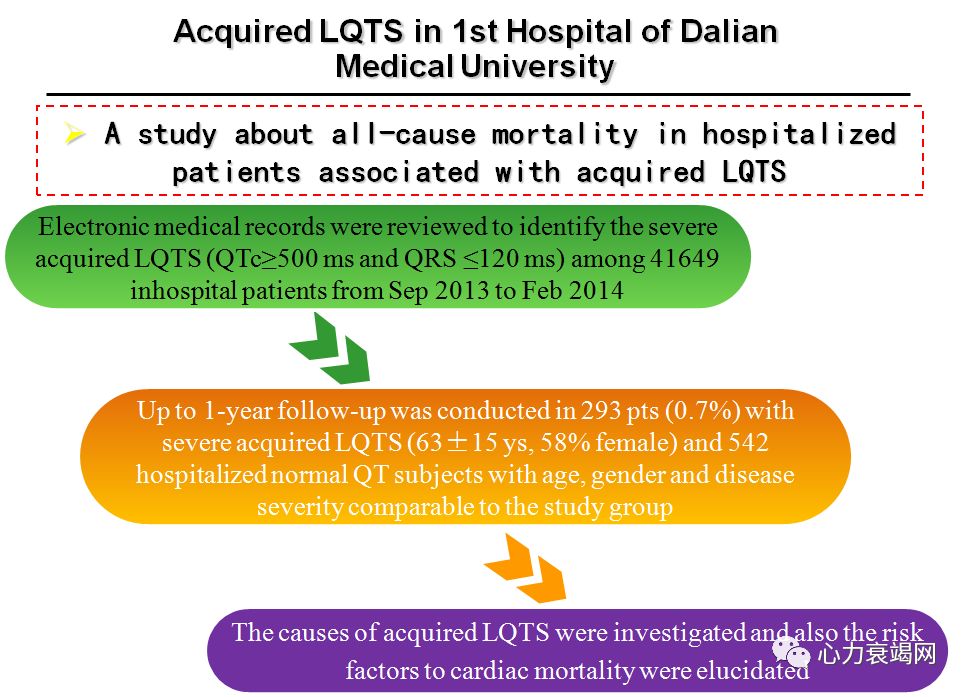
QT间期延长:不论女性或男性,QTc>500ms 都属于明显的异常; QTc改变>600ms,可能导致严重的心律失常
QT间期延长、T波和(或)u波异常、早搏后的代偿间歇及心率减慢时易于发生尖端扭转型室速 (TdP)和心源性猝死
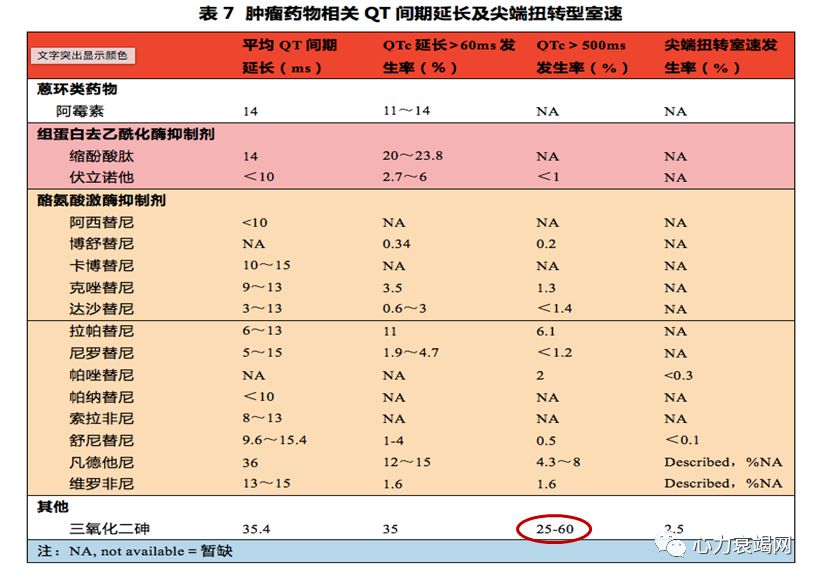
心肌细胞毒性:导致心肌重构和电重构,一般是慢性作用(阿霉素类、曲妥珠单抗)
作用于相关离子通道,一般用药后很快就能引起QT间期延长
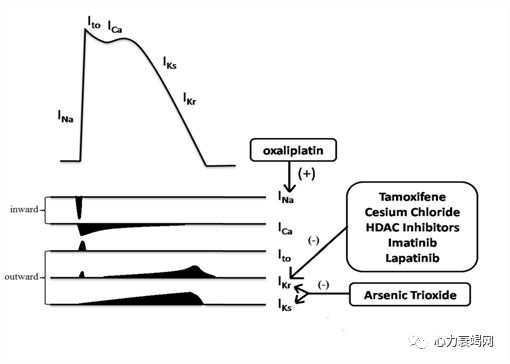

对所有患者,均需在启动治疗前采集12导联心电图,测量其QT间期,并计算心率校正的QT间期(QTC)
对QT间期延长、心脏疾病、合用可致QT间期延长药物、心动过缓、甲状腺功能异常及电解质紊乱患者,抗肿瘤治疗期间需密切随访12导联心电图
对治疗期间QTC>500ms、QTC延长超过60ms或新发心律失常患者,应考虑中止或调整抗肿瘤方案。
对药物致QT间期延长患者,需避免低钾血症、显著心动过缓,慎防尖端扭转型室速
潜在QT间期延长作用的化疗药物应尽量避免与其它可致QT间期延长的药物合用
Eur Heart J2015;36:2793–2867
常见心律失常——房颤
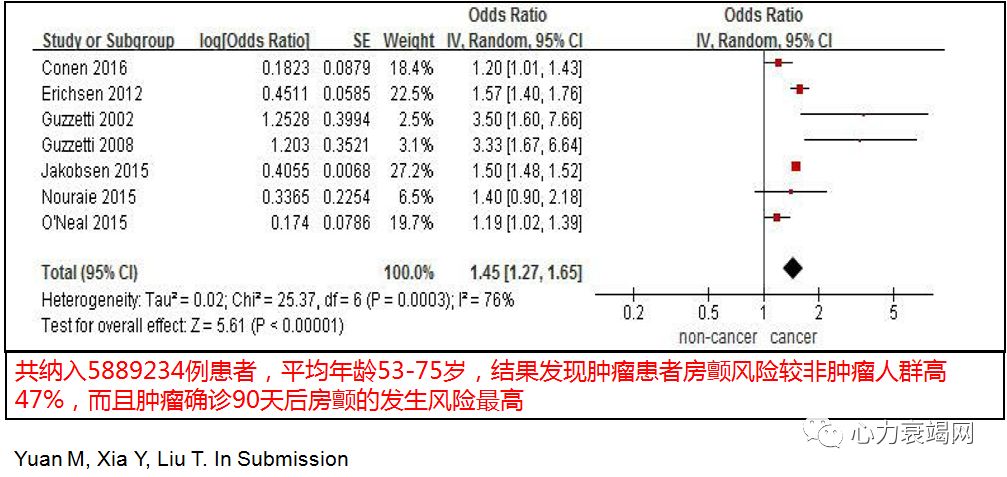
电解质紊乱、代谢紊乱、炎症反应等
自主神经功能障碍(癌痛/情绪)
细胞毒性药物
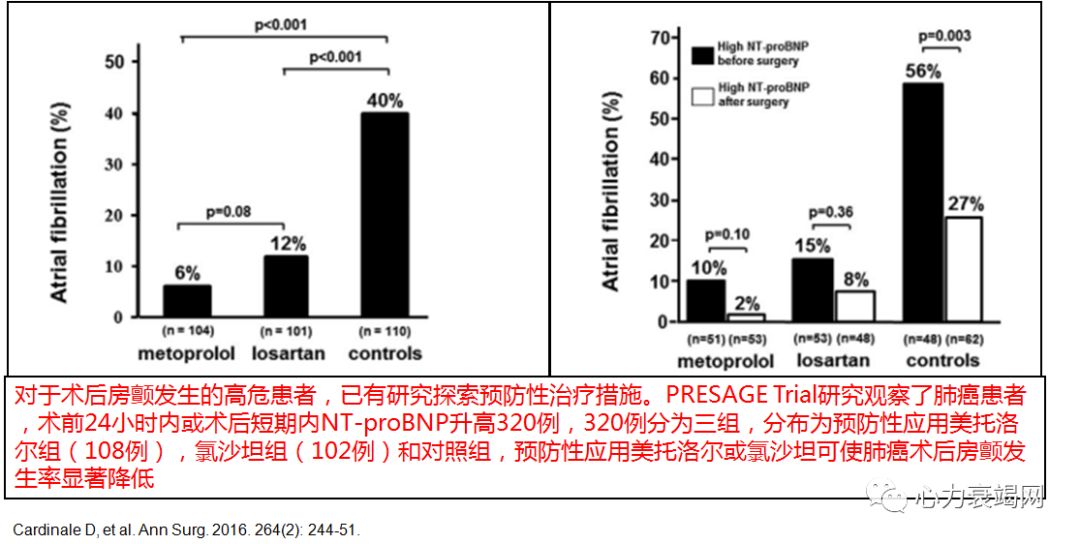
外科术后房颤:开胸手术(尤其是肺叶切除术后)更为常见,肺癌术后房颤的发生率可达30%
术后系统性炎症、氧化应激、交感神经系统亢进
Farmakis D, et al. JACC, 2014,63:945-53.
高龄、男性、恶性肿瘤的分期、手术时间长短、是否发生手术并发症、心血管基础疾病等
NT-proBNP升高
左室舒张功能降低……
Ai D, et al. J CardiothoracVascAnesth. 2015,29:1127-30
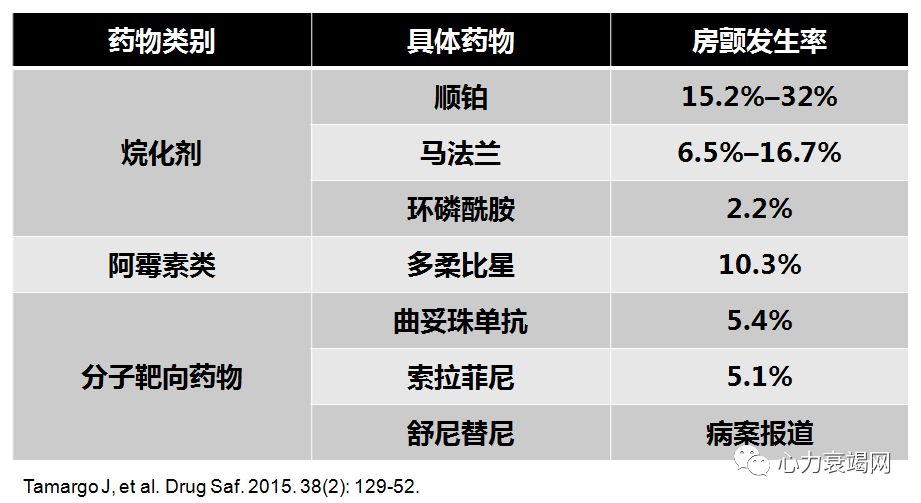
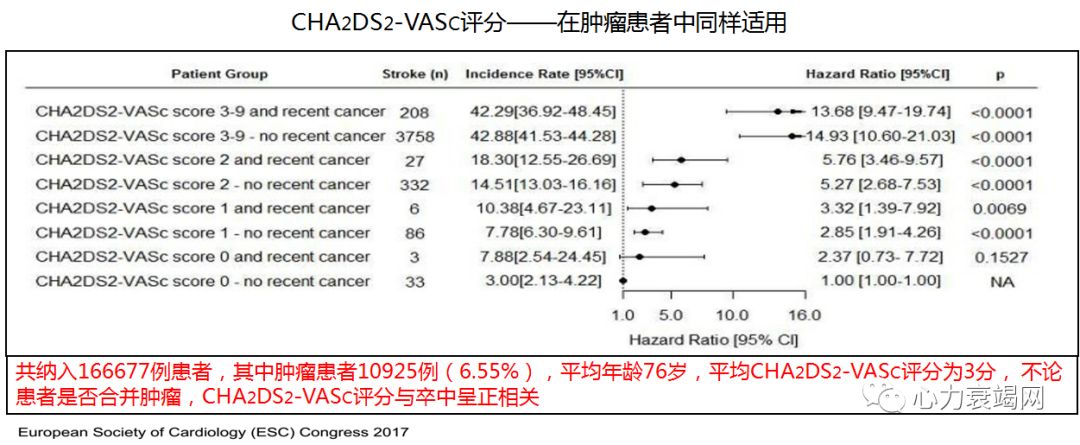
CHA2DS2-VASc≥2分的患者,如血小板计数>50000/mm3,可考虑应用维生素K拮抗剂,并进行有效的抗凝管理(INR达标时间大于70%)
即使是卒中低风险的房颤患者,因合并肿瘤时VET风险增加,也应考虑抗凝
抗凝前应充分评估,包括超声心动图、合并症、出血风险、患者意愿和依从性
低分子肝素(LMWH)—— 短到中期治疗方案
维生素K拮抗剂(华法林)——INR波动较大时推荐使用LMWH
新型口服抗凝药(NOACs)——抗凝作用及安全性有待评价
2016 ESC Position Paper on cancer treatmentsand cardiovascular toxicity developed under the auspices of the ESCCommittee for Practice Guidelines
常见心律失常——缓慢型心律失常
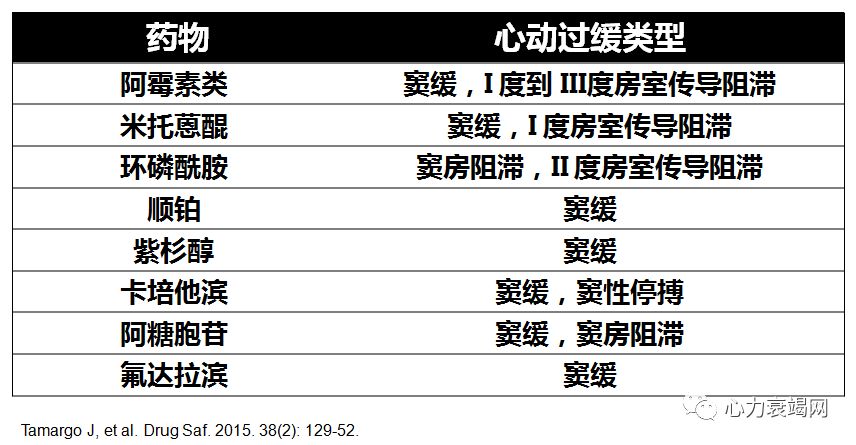
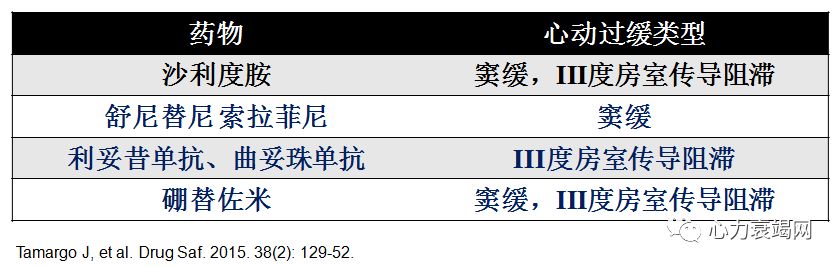
心肌及心脏传导系统损害(阿霉素类等)
直接刺激迷走神经(多柔比星)
诱发电解质紊乱(铂类化合物)
β受体阻滞剂样作用(米托蒽醌)
曲妥珠单抗可选择性抑制HER-2,用于乳腺癌的治疗,其不良反应为房室传导阻滞
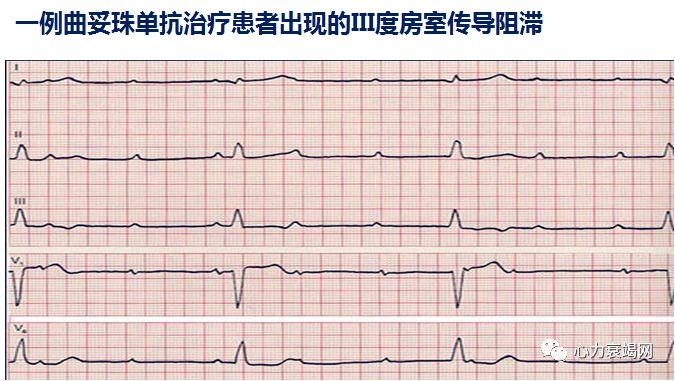
很多导致心动过缓的药物能够延长QT间期,而心动过缓是TdP的危险因素,因此在监测心率时,应同时密切关注QT间期的变化;
对于高龄、有基础心脏病、电解质紊乱的患者,应在用药前后积极监测;
对于紫杉醇类药物,用药一小时内应密切监护心律;
对于沙利度胺引起的心动过缓,如心律在50-60次/分且相关症状者,无需停药。对于心律<50次/分的患者,应立即停药。对于不能停药的患者,可考虑永久起搏器植入
肿瘤与心律失常密切相关,尤其对于ALQTS和房颤的管理与治疗在很多患者中被忽视;加强抗肿瘤治疗前评估、治疗中及治疗后监测,“防”重于“治”
在目前心律失常机制理解和技术进步不断深入的情况下,肿瘤科与心血管科紧密合作,很多患者可以得到个体化的合理解决
肿瘤心脏病学作为新兴交叉学科,未来需要多学科、多中心临床研究提供询证医学证据,指导临床决策,不断提高患者的预期寿命和生活质量
