

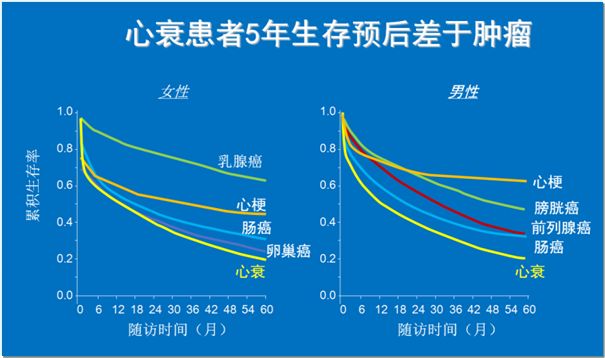
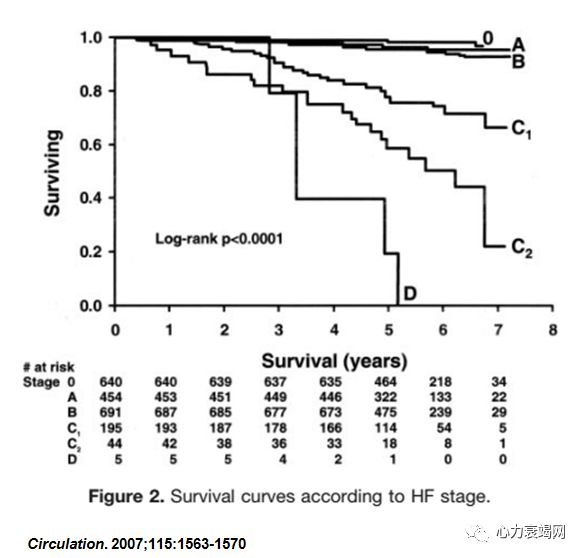
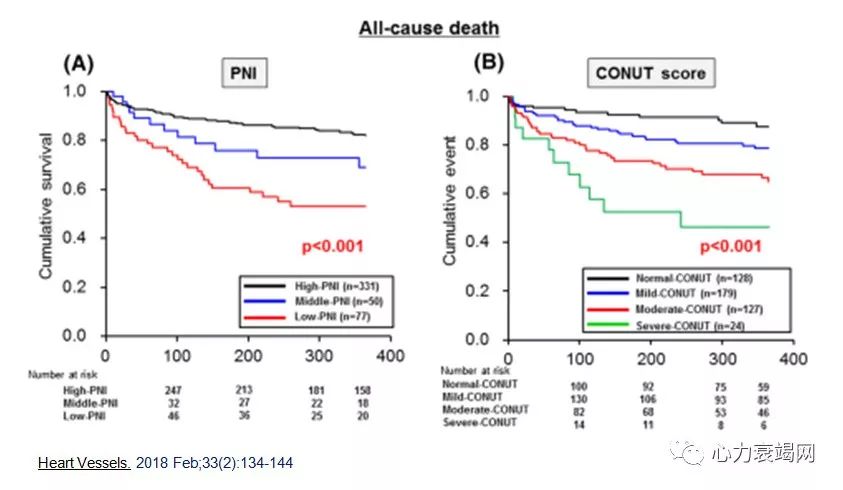
心力衰竭是各种心脏病发展的严重阶段,即使综合优化治疗,患者的预后仍很差,5年存活率与恶性肿瘤相当。

➤ 其定义尚无统一
因不同研究人群、采用诊断标准差异较大
HF 患者中营养不良比例高(16-90%)
尤其是进展期急性失代偿性HF,发生率高达75-90%
HF中恶病质约占5-15%
Heart FailRev. 2016Sep;21(5):549-65.
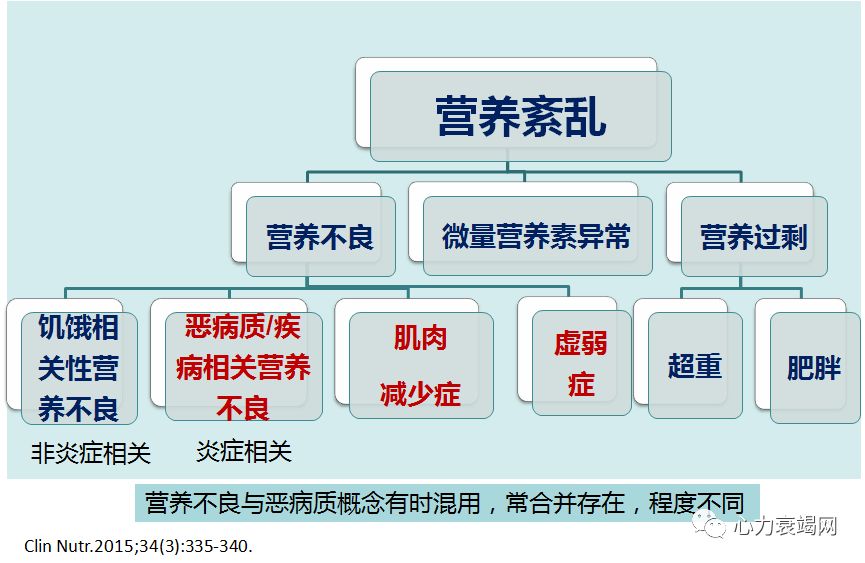
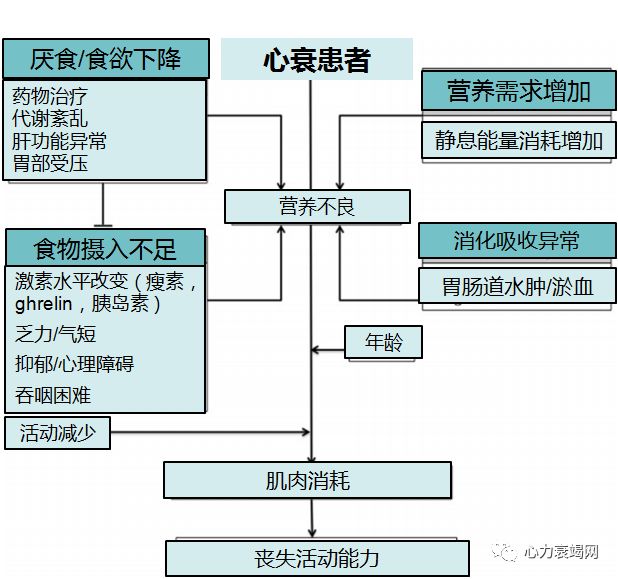
定义:在既往6-12 个月内,非故意、非水肿性体重减轻≥6%的总体重。
恶病质是一种影响身体各个部分即骨骼肌、脂肪组织(能量储存)和骨组织(骨质疏松)的全身性消耗过程。
见于5-15%的心衰患者,特别是HFrEF和较严重的患者HF最严重的并发症,不良预后的独立预测因素。18个月后的死亡率通常在50%。
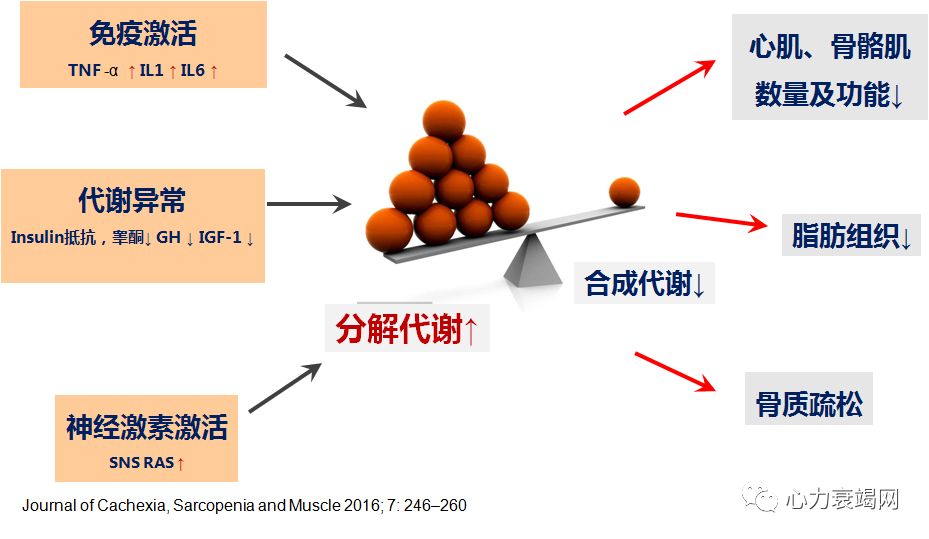
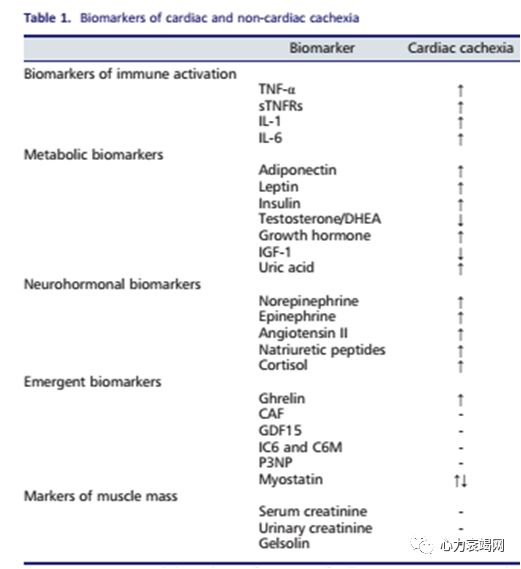
脑肠肽(Ghrelin):促进GH释放、进食
VI 型胶原转换相关多肽(IC6and C6M) :肌肉体积改变
P3NP:III型前胶原N末端多肽,反映肌肉合成代谢
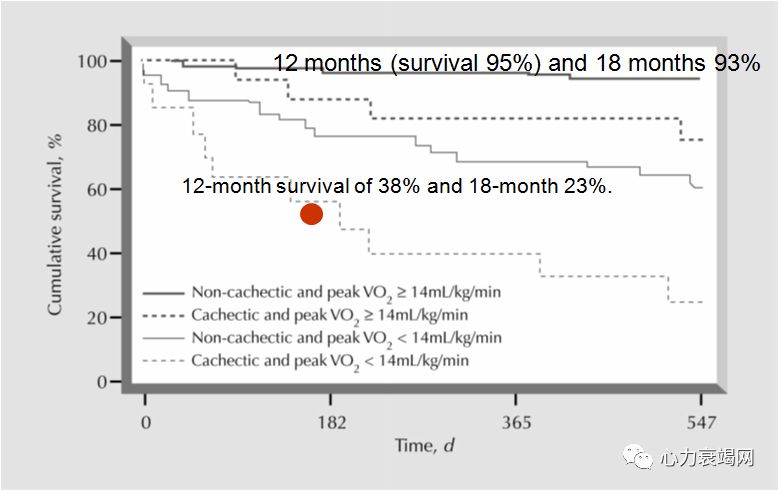
恶病质阶段,干预效果差,因此有必要早期评估心衰患者的营养状况,进行营养干预
心衰患者的管理目标是提供一个“ 无缝的”医疗保健体系,这个体系包括贯穿医疗保健的全程。
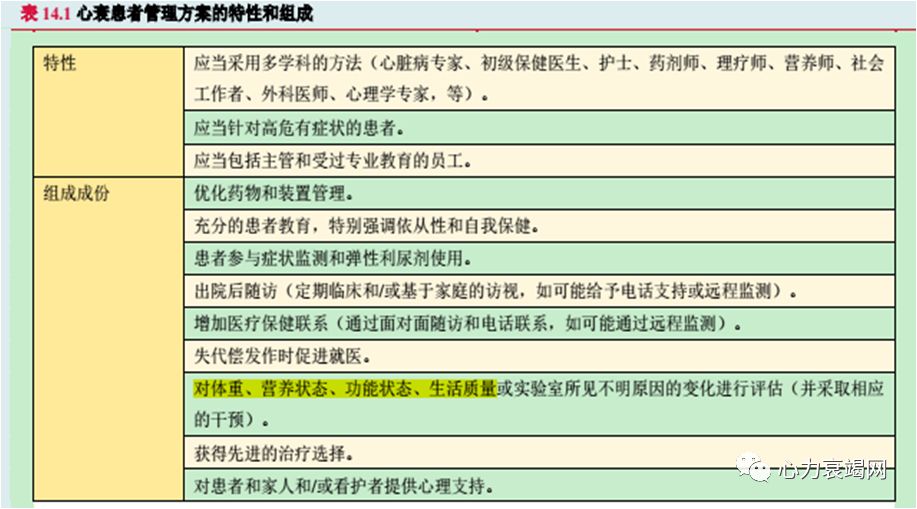

“营养风险” 包含两层含义:
a.有营养风险的患者不一定存在营养不良,但如果忽视营养风险,有可能进展为营养不良,进而影响预后;
b.有些有营养风险的患者已经存在营养不良。
不要坐等患者出现营养不良再去干预
目前临床上进行营养风险筛查的方法有多种,主要为使用单一指标和复合指标两类,但尚缺乏公认的营养风险筛查工具。
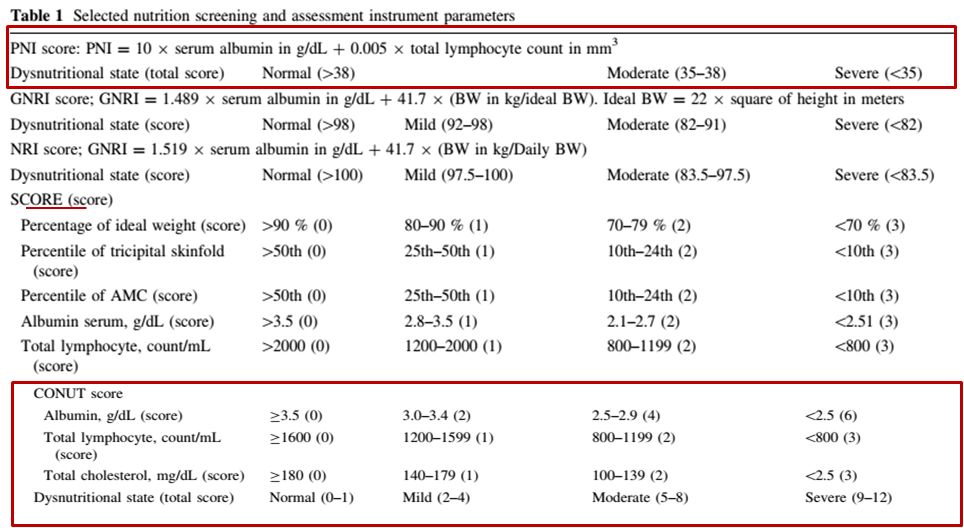
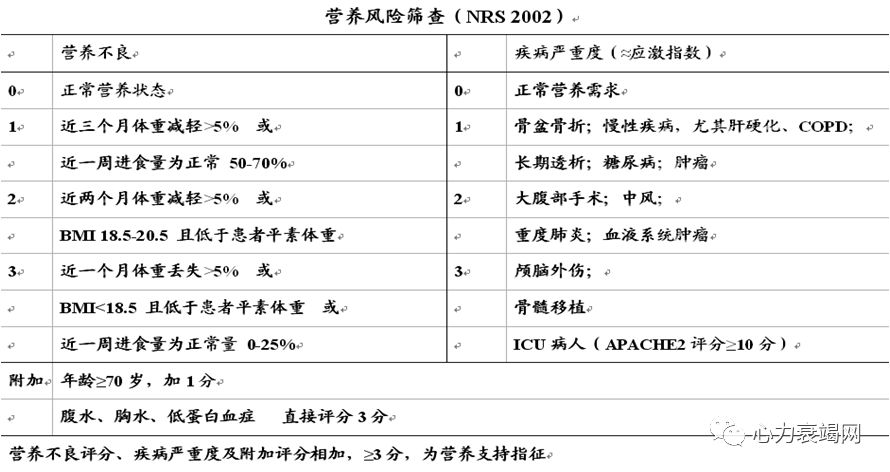
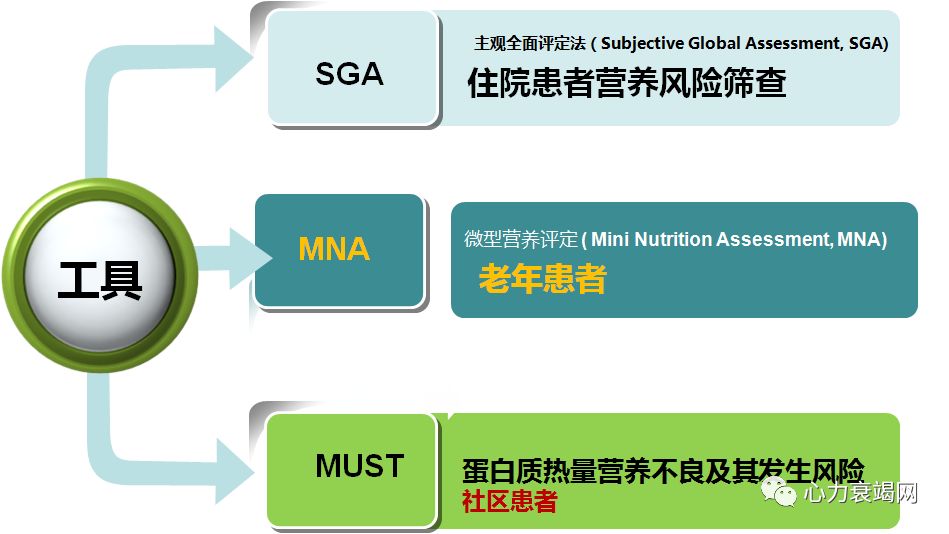

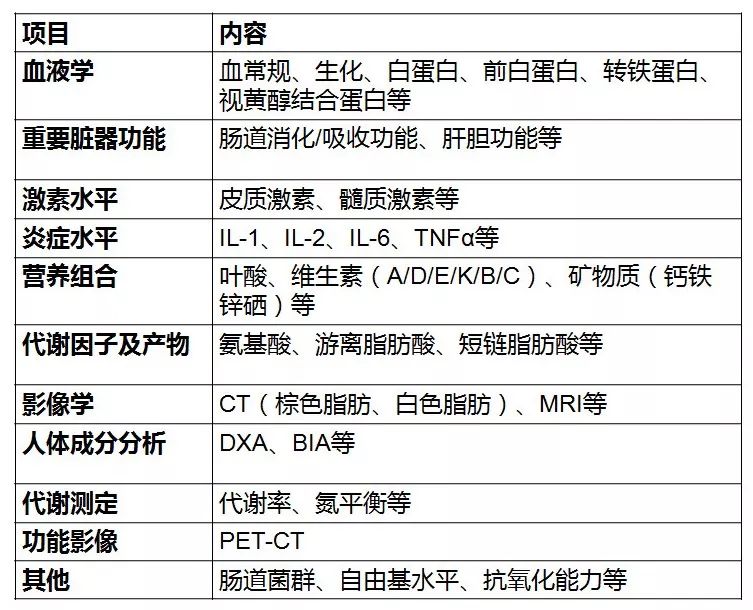
营养状况正常但有营养风险(NRS-2002评分≥3分);
中度营养不良预计营养摄入不足>5d;
重度营养不良;
合并营养摄入不足、生长发育迟缓及停滞的儿童和青少年;(强烈推荐)
有手术指征的患者合并营养不良或有营养风险时,推荐先纠正营养不良,以降低手术风险。
供给细胞代谢所需要的能量与营养底物,维持组织器官结构与功能;
采用通过营养素的药理作用调理代谢紊乱,调节免疫功能, 增强机体抗病能力,从而影响疾病的发展与转归,这是实现重症病人营养支持的总目标;
合理的营养支持,可减少净蛋白的分解,改善潜在和已发生的营养不良状态,防治并发症。
营养支持应在充分复苏、获得稳定的血流动力学状态、纠正严重的代谢紊乱的前提下及早开始
血流动力学不稳定时,患者需要积极的血流动力学支持治疗,以维持细胞灌注,应暂停肠内营养直至复苏完全(或)病情稳定
对于重症患者,肠鸣音存在与否以及是否排气排便均不影响开始肠内喂养
(1)代谢车:静息能量消耗(REE)
(2)Harris Benedict 公式计算:
男性:BEE=66.47+13.75W+5H-6.76A
女性:BEE=655.10+9.56W+1.85H-4.6A
(W=体重(kg),H=身长(cm),A=年龄(a))
(3)膳食调查
(4)能量估算:
缓解期:25-30kcal/kg·d
活动期:增加8-10%

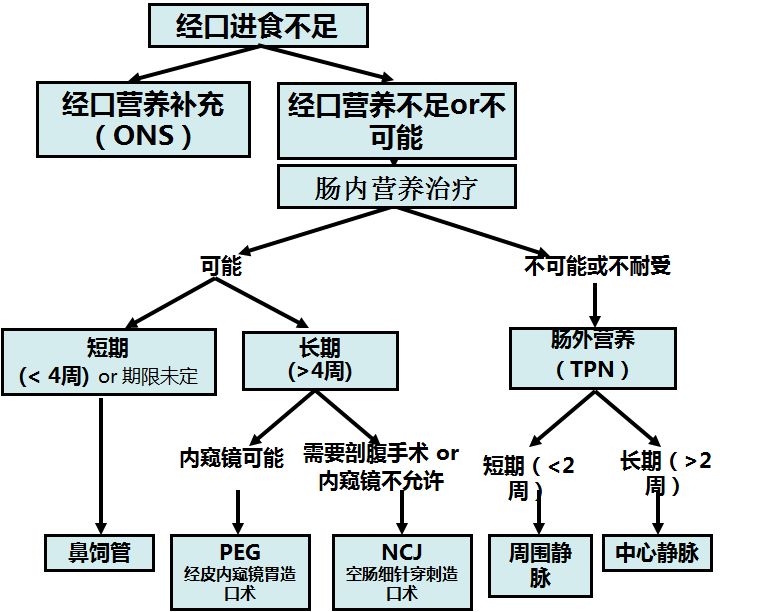
推荐意见:只要胃肠道解剖与功能允许,并能安全使用,应积极采用肠内营养支持(EN)。
推荐意见:任何原因导致胃肠道不能使用或应用不足,应考虑肠外营养(PN),或联合应用肠内营养(PN,PN+EN)。
重症心衰患者为减轻心脏负荷,需控制输入液体总量、控制体内钠水潴留
营养支持的前后应严密监测与心功能相关的指标。如血糖、血脂、中心静脉压、肺毛细血管楔压、水电解质和酸碱平衡、24小时出入量等
EN时密切观察腹部情况。及时评估营养支持的效果,并调整配方
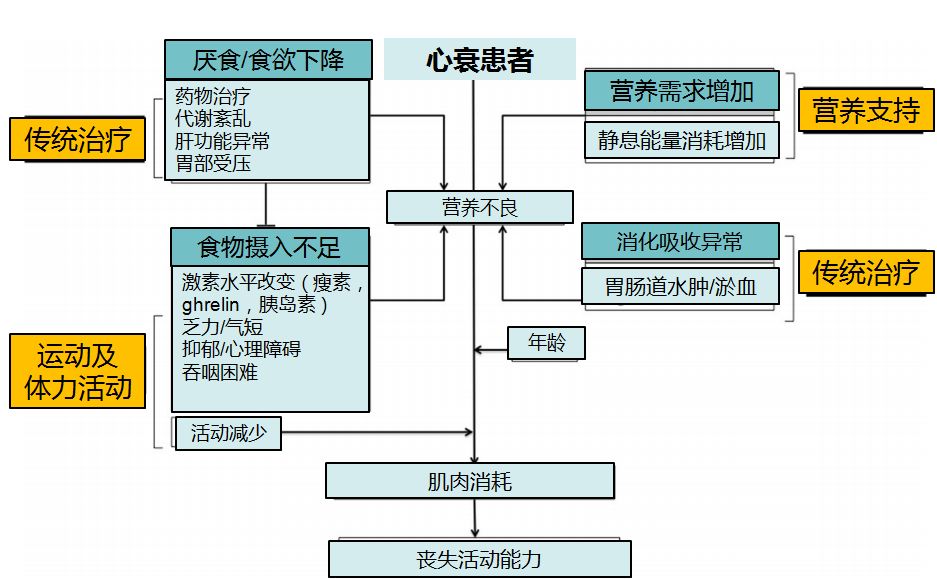

心衰患者营养不良发生率高,尤其是进展期心衰常伴有恶病质
营养不良导致心衰合并症及死亡率增加
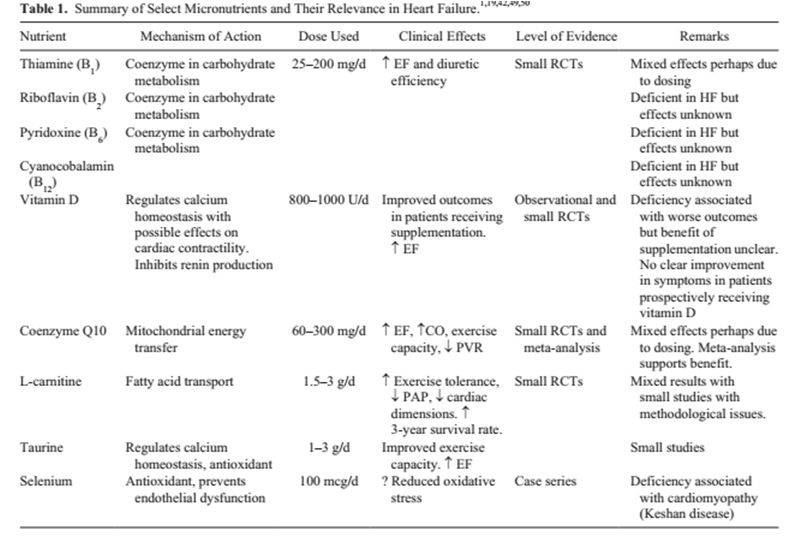
营养评估及营养支持是心力衰竭管理的重要组成部分
营养风险筛查及营养评估有助于识别高危患者,尽早进行营养干预
重症心衰患者营养支持应控制总液体量、以肠内营养支持为主,并监测心功能指标及腹部情况
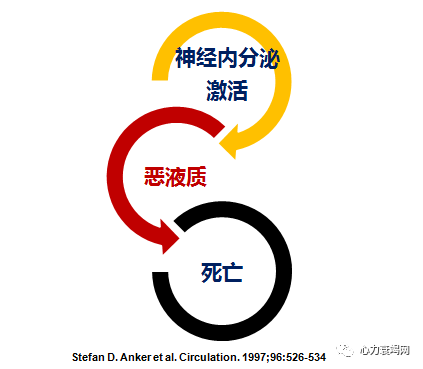
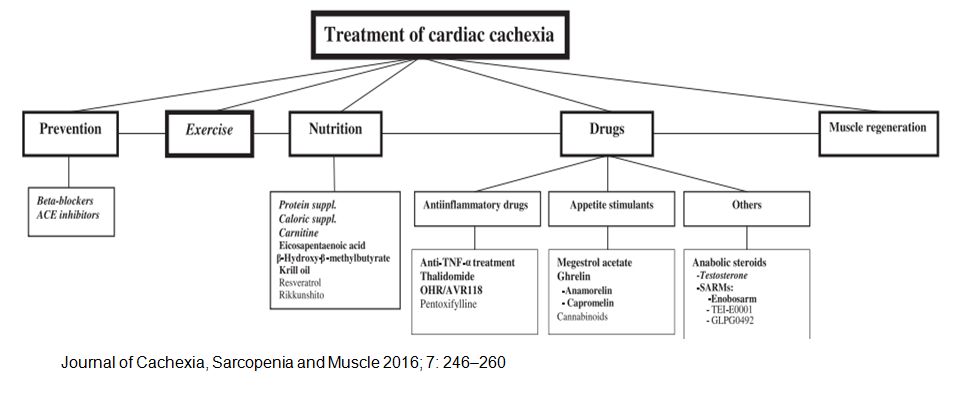
恶病质的发生与全身炎症反应、代谢异常、神经激素激活有关恶病质的治疗以预防、运动、营养支持为主,缺乏有效药物
