


流行病学

心肌炎的病因[1]
病毒感染是北美、欧洲心肌炎最重要的病因
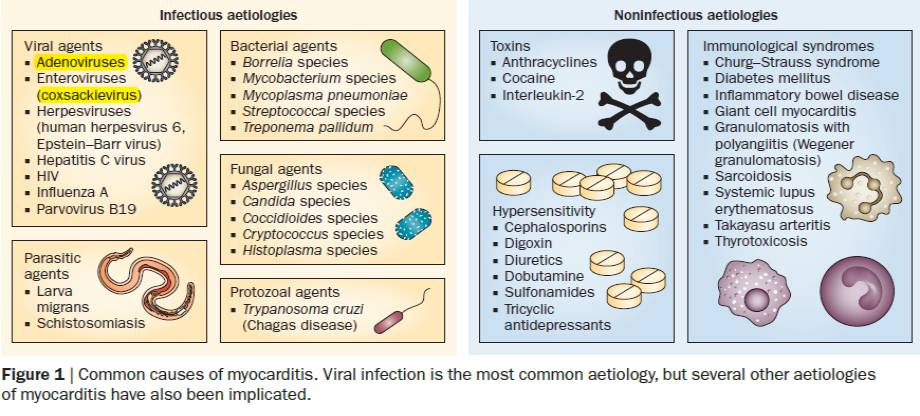
发病机制

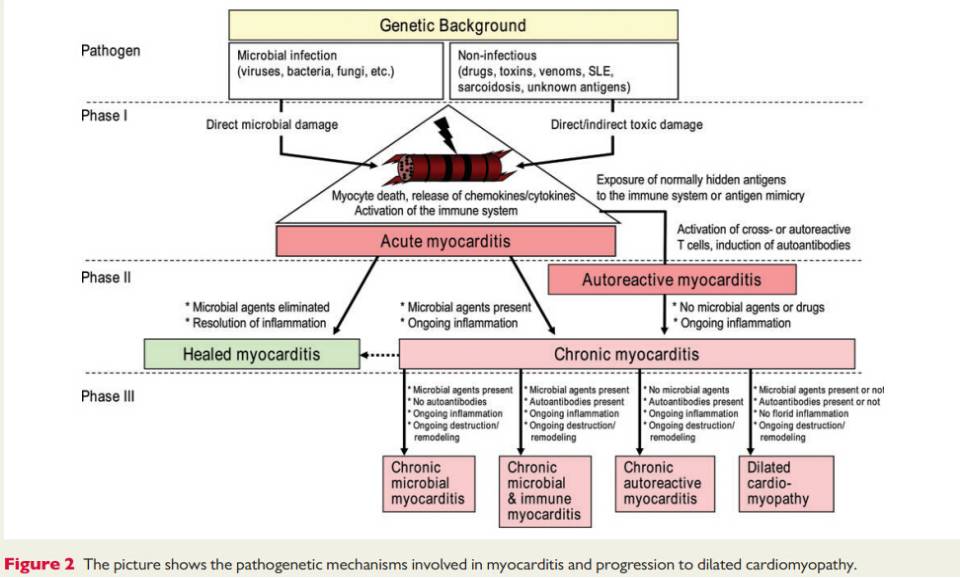
心肌炎临床表现[2]
急性胸痛、心包炎或心肌缺血样
新出现(数天到3个月)或加重的:静息或劳力的呼吸困难和/或乏力,伴或不伴左和/或右心衰体征
亚急性/慢性(>3个月)或加重的:静息或劳力的呼吸困难和/或乏力,伴或不伴左和/或右心衰体征
心慌,和/或不能解释的心律失常症状和/或晕厥,和/或心脏骤停
不能解释的心源性休克
暴发性心肌炎临床表现
暴发性心肌炎
临床特点:心衰症状显著(乏力、呼吸困难、浮肿)、严重心律失常、心脏骤停、急骤进展(1-2天内)发热、起病前2周内病毒感染史。
血流动力学:严重血流动力学紊乱,大剂量(>5 µg/kg/min 多巴胺或多巴酚丁胺)或机械循环支持。
并发症:严重心衰、心源性休克、呼衰、肝肾功能不全、神经系统异常。
预后:临床危急、需积极血流动力学支持,远期预后佳。
急性重症心肌炎
临床特点:心衰进展较慢(数周-数月),无发热。
血流动力学:血流动力学稳定或小剂量(<5 µg/kg/min多巴胺或多巴酚丁胺。
并发症:有心衰、无循环衰竭或休克。
预后:亚临床起病、易进展为扩张性心肌病、远期预后不佳。
辅助检查
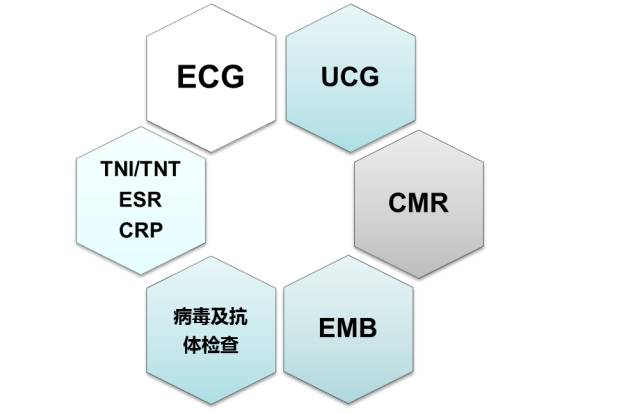
实验室检查

不推荐常规行血清病毒学检查:
阳性并不能说明心肌病毒感染,只是提示外周免疫系统对于病原的反应
不侵犯心肌的病毒感染可以产生类似的化验结果;
研究表明病毒血清学检查与EMB之间没有关系
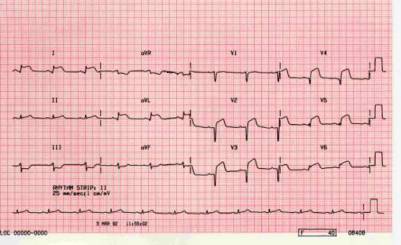
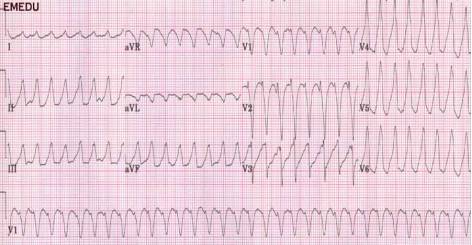
ECG改变
通常有异常改变,但既不特异也不敏感;需要注意一些特殊改变可以提示心肌炎
1、窦性心动过速
2、非特异性ST段下移、T波倒置
3、房室传导阻滞、左束支阻滞
4、ST段抬高类似于急性心包炎
5、ST段抬高类似于急性心肌梗死
6、QRS波增宽、病理性Q波(预后不良
新发的室速、Ⅱ°Ⅱ型及 Ⅲ°AVB 提示巨细胞性心肌炎的可能,应引起关注
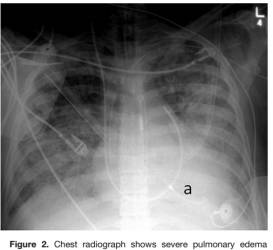
胸 片

肺水肿表现
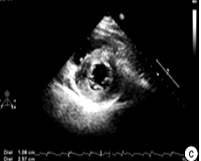
心脏超声
诊断室壁运动异常、左右心室大小及功能、心包积液、瓣膜返流
血流动力学恶化时需复查

冠状动脉造影
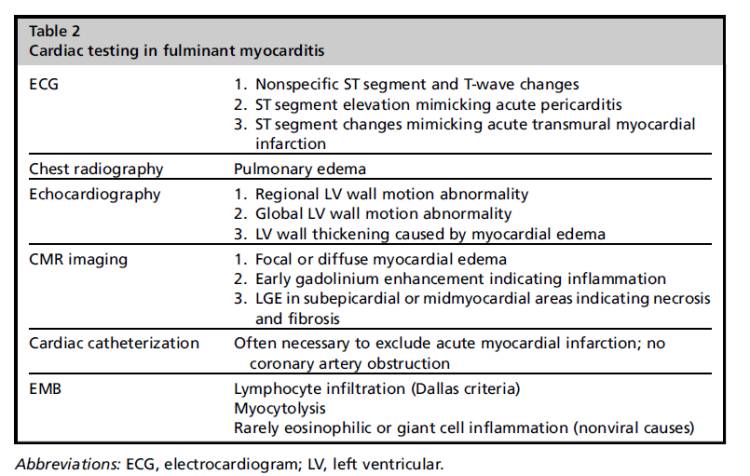
心脏磁共振
最重要的无创性检查方法,显示3种心肌病变
诊断准确性:符合2-3个标准时达78%,仅LGE时68%发病7天后MRI敏感性高于发病初期
指导心肌活检部位
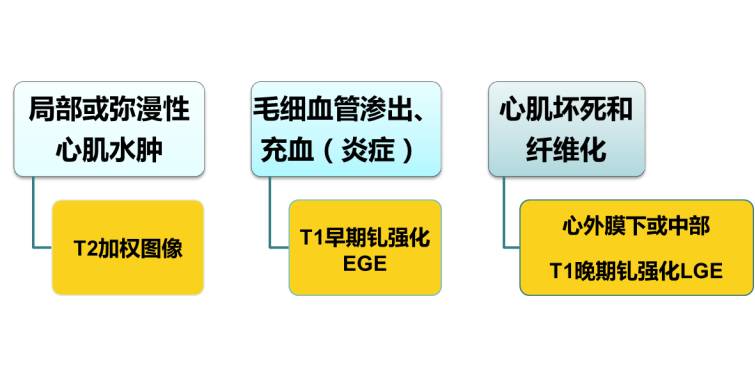

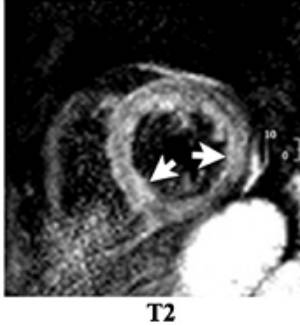

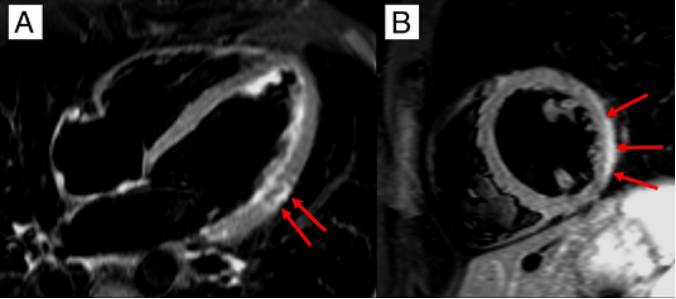
路易斯湖MRI诊断标准

心内膜下心肌活检EMB[2]
EMB:心肌炎诊断的金标准,有创、敏感性低
新的观点:心内膜活检应更多用于评估病情及选择治疗
推荐用于:
①暴发性心肌炎、炎症室性心律失常、进展性AVB
②鉴别淋巴细胞心肌炎、巨细胞性心肌炎、嗜酸细胞性心肌炎(后两者需免疫抑制剂)(I类推荐)
③推荐在用免疫抑制剂前行EMB
MB:常规镜检 + 免疫组化染色 + 病毒PCR(心肌和血液)
右室或左室取至少3个心肌标本,1-2mm大小,室温下立即固定于10%福尔马林(光镜);其他组织快速冻于液氮,-80°保存,或室温存放于RNAlater tubes(病毒PCR)
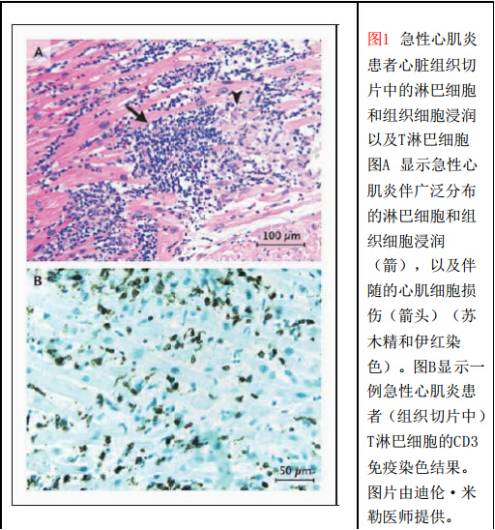
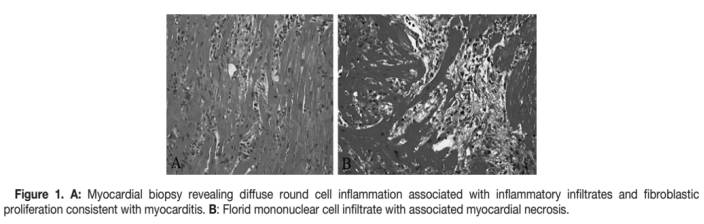
Dallas病理学标准:常规染色的心脏组织切片中,存在炎症细胞浸润,伴或不伴相关心肌细胞坏死(图1A)
局限性:判读结果的多样性,缺乏预后价值和敏感性低,部分是抽样误差所致
新的病理检查:如抗CD3、抗CD4、抗CD20、抗CD68和抗人类白细胞抗原(HLA)等细胞特异性免疫过氧化酶染色为依据 (图1B)
敏感性较高,可能有预后价值
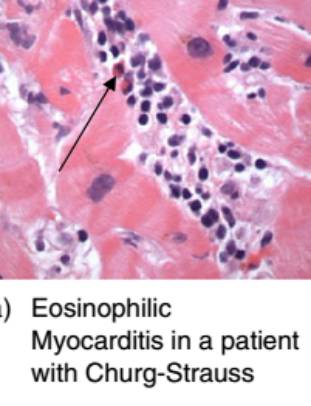
嗜酸细胞性心肌炎:
特点:心肌内以嗜酸性粒细胞浸润为主
可伴有全身性疾病,如嗜酸细胞增多综合征、Churg-Strauss综合征(变应性肉芽肿综合征)、Löffler心内膜心肌纤维化、癌症以及寄生虫、蠕虫或原虫感染
临床表现:心力衰竭、心内膜和瓣膜纤维化以及心内膜血栓
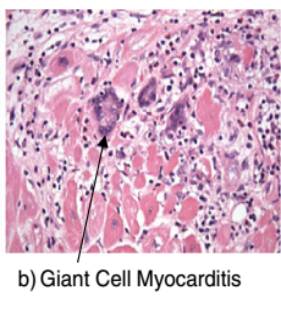
巨细胞性心肌炎
特殊的病理表现:
①非肉芽肿性多核巨细胞浸润;
②淋巴细胞、组织细胞、嗜酸性细胞等多种炎性细胞浸润;
③局灶或凝固性坏死,边缘有上述细胞浸润。
临床:起病快,病死率高,或需心脏移植。
罕见,认为是自身免疫性疾病,与多种自身免疫病、胸腺瘤和药物过敏有关。
一旦怀疑该病应尽快进行心内膜活检。
诊断标准[2]
ECG/Holter/负荷试验
I~III度AVB、束支传导阻滞、ST段或T波改变(ST段抬高或非抬高,T波倒置)、窦性停搏、室速或室颤和停搏、房颤、R波减小、室内传导组织(QRS增宽)、病理性Q波、低电压、频发早搏、室上性心动过速。
心肌细胞溶解的标志物
TNI或TNT升高
心脏影像示功能和结构异常(超声/血管造影/CMR)
新发的,不能用其他原因解释的左室和/或右室结构和功能异常:节段性室壁运动异常或整体收缩或舒张功能异常,伴或不伴心室扩张、室壁厚度增加、心包积液及腔内血栓。
CMR显示的组织特点
水肿和/或典型的心肌炎LGE。
临床拟诊心肌炎[2]
1+1:≥1个临床表现+≥1个诊断标准
需排除:冠状动脉病变,已知的已存在的心血管疾病或可以导致临床症状的心外因素(如瓣膜病、先天性心脏病、甲亢)。
符合诊断条件越多怀疑性越高。
如果没症状,需要≥2条诊断标准。
暴发性心肌炎临床表现
暴发性心肌炎
临床特点:心衰症状显著(乏力、呼吸困难、浮肿)、严重心律失常、心脏骤停、急骤进展(1-2天内)发热、起病前2周内病毒感染史。
血流动力学:严重血流动力学紊乱,大剂量(>5 µg/kg/min 多巴胺或多巴酚丁胺)或机械循环支持。
并发症:严重心衰、心源性休克、呼衰、肝肾功能不全、神经系统异常。
预后:临床危急、需积极血流动力学支持,远期预后佳。


鉴别诊断
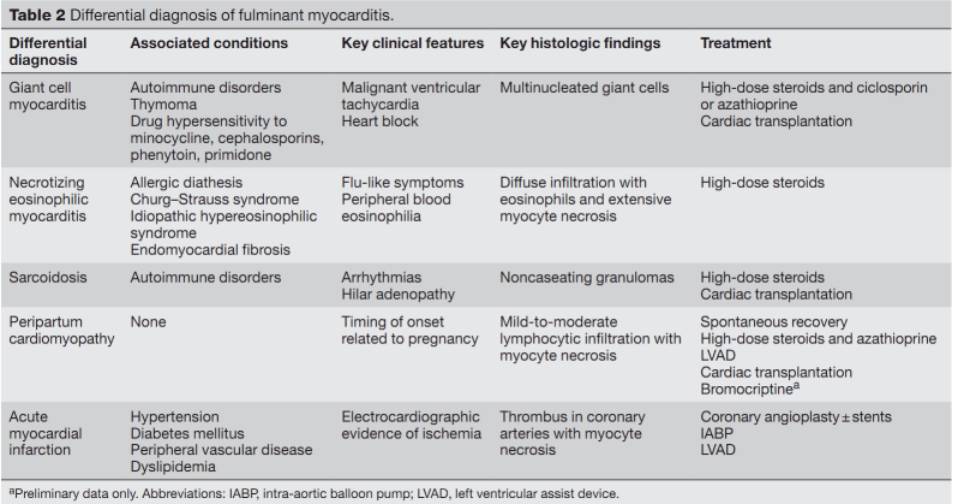
暴发性心肌炎诊治流程[3]
治疗原则
主要是支持治疗、危重患者转院(血流动力学监测、EMB)
纠正心衰,抗心律失常(相应的指南)
循环不稳定的危重病人需要积极的辅助装置
主动脉内球囊反搏IABP
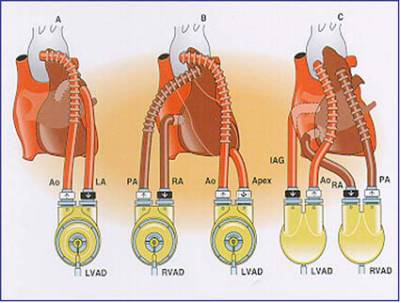
左室辅助装置VAD/Bi-VAD
体外膜肺氧合ECMO
起搏治疗
稳定后长期改善心室重构治疗
抗病毒治疗以及免疫治疗仍有争议
药物治疗
一般治疗:心电、血压、血氧监护、记出入量、机械通气
袢利尿剂:静脉速尿,减轻肺水肿/肺淤血
正性肌力药:
多巴酚丁胺:β1激动剂,β2和α受体激动较少
心肌收缩力↑、血管阻力↓,PCWP↓, 缺点:可致心律失常,易耐药
米力农:心肌收缩力↑、SV ↑、CI↑,血管阻力↓,PCWP ↓、SBP↓
注意:低血压慎用,必要时联合升压药,致心律失常少于多巴酚丁胺
升压药:去甲肾上腺素及多巴胺,用于顽固性低血压
缺点:心肌耗氧量↑,不增加CI
主动脉内球囊反搏IABP
IABP是经股动脉在左锁骨下动脉以远与肾动脉近端的降主动脉内的置入球囊,导管另一端连接反搏仪。
舒张期,气囊迅速充气膨胀,增加舒张期峰压。
收缩期主动脉瓣开放的瞬间,气囊放气,减轻左室的后负荷,减少左心室壁张力及左室做工和耗氧。
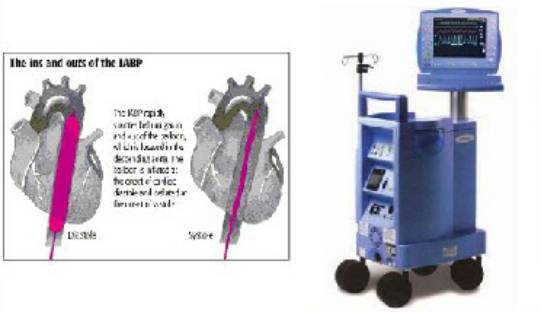
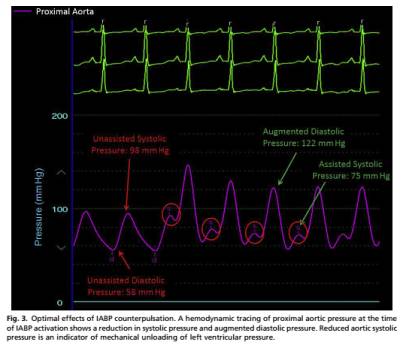
优点:
收缩压降低
左室舒张末压降低
心肌耗氧量降低
心输出量增加 10%~40%
冠状动脉峰值血流速度增加
缺点:
心输出量的增加并不非常明显(10%~40%)
仅限于左室辅助
不能解决氧合
下肢缺血
体外膜肺氧合ECMO
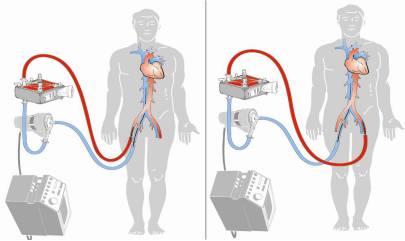
V-A ECMO是将血液从体内引到体外,经膜式氧合器(膜肺)氧合再用离心泵将血灌入体内。全部或部分代替心肺功能。(平均5-8天)
作用:降低前负荷、升压、改善氧合和及组织代谢
优点:床旁手术、快速建立(20-30min),经皮技术、局麻唯一经皮LV+RV+肺脏支持
缺点:LV 后负荷↑→ LVEDP、室壁张力↑→ LAP↑→ 肺水(可联用IABP、LVAD)
AMI
心肌炎
低心排
术后心肌顿抑
心脏移植前后
ECMO 使用时机未统一,出现以下情况时,推荐早期使用:
正性肌力药和/或IABP使用下难治性休克,有灌注不足表现
致命性室性心律失常
需要心肺复苏(除非时间极短)
VAD/Bi-VAD用人工制造的机械装置,部分或完全替代心脏泵血功能,保证全身组织和器官的血液供应
VAD的流入管道可采用左心房或左心室心尖部插管,流出管道通过一段人工血管与升主动脉吻合
优点:降低心脏作功、氧耗,有助于心肌恢复
缺点:需要手术,创伤大,但可以长时间维持,甚至作为长期替代治疗
并发症:感染、败血症、血栓栓塞和出血
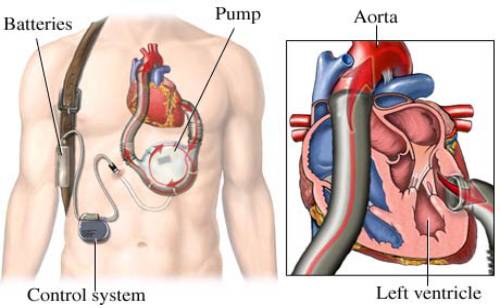
经皮左心室辅助装置Impella
适用于心内科、外科;
由控制台、心室辅助装置和净化系统组成
轴流泵,使用周期5-7天;
血液从左心室流入心室辅助装置,从升主动脉流出;
优点:减少左心室工作,使心脏得到有效休息;增加心排量。
缺点:不提供 RV 及肺脏的支持。
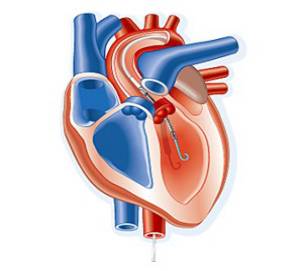
心室辅助装置分3种规格:
----Impella LD (004410)
外科手术放置,流量5L/min
----Impella 5.0 (004412)
股动脉切开,流量5L/min
----Impella 2.5 (004413)
股动脉穿刺,流量2.5L/min

31岁, 男性,暴发性心肌炎
心源性休克、急性肾衰、肝衰,EF25%
大剂量血管活性药物
气管插管、抗病毒、免疫球蛋白无效
D4:Impella2.5*5天
D5:ECMO*3天
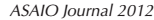
心脏移植
危重心肌炎患者的最终选择
因为有可能恢复,急性期应推迟心脏移植
在血流动力学不稳定患者,包括巨细胞性心肌炎,如果理想的药物和机械辅助装置无效时可以考虑
与缺血性或其他原因心肌病相比,移植排异反应较重
在移植心脏中也可再发心肌炎
心律失常
急性期出现的心律失常和传导阻滞,与其他心脏病处理情况相同:
抗心律失常药物
临时起搏
强烈建议在决定安装永久起搏或ICD前,先经过一段时间、观察心脏功能恢复情况
血流动力学稳定后
心肌炎伴心力衰竭者
ACEI:小剂量起始,滴定至最大耐受剂量
密切监测:肾功能、高钾及血管性水肿
相对禁忌症:低血压、肾衰竭、高血钾、双侧肾动脉狭窄、肝衰竭
β受体阻滞剂:改善急性心肌炎患者生存率.
时机:在ACEI剂量稳定后使用,液体潴留改善
禁忌症: 哮喘、严重阻塞性肺病、AVB、显著的心动过缓、低血压
地高辛:用于房颤患者控制心室率,显著左室收缩功能不全、在ACEI和β受体拮抗剂使用后仍有症状,生存率无改善。
禁忌症:肾衰、AVB
螺内酯:减少扩心病患者心肌纤维化。推荐用于心肌炎伴EF≤35%和症状性心力衰竭。禁忌症:肾功能不全、肌酐>2.0 mg/dl,高血钾
抗病毒治疗
目前尚无认可的针对肠道病毒的抗病毒疗法。
阿昔洛韦、更昔洛韦、伐昔洛韦也许可考虑用于疱疹病毒感染,尽管其有效性在心肌炎中尚未证实。
干扰素的初始数据显示它能消除左心室功能不全患者的肠道病毒及腺病毒基因组,可改善NYHA心功能分级,尤其对肠道病毒感染改善10年预后。
建议在决定启用特定抗病毒疗法时咨询感染科医师。
免疫抑制治疗
RCT示急性淋巴细胞性心肌炎的常规治疗中,免疫抑制无益。
免疫抑制治疗前应行EMB(PCR)排除急性感染
免疫抑制治疗考虑用于确诊自身免疫性心肌炎(感染阴性)、无禁忌症,包括巨细胞性心肌炎、心脏结节病和与已知心外自身免疫性疾病相关的心肌炎
激素治疗的适应症:合并心室功能不全和/或心律失常的心脏结节病、合并心衰或心律失常的病毒阴性的嗜酸粒细胞性或中毒性心肌炎
免疫抑制可考虑在个体化、感染阴性、对标准治疗无效的淋巴细胞性心肌炎,且无禁忌症者
EMB 随访指导免疫抑制强度和治疗时间
免疫球蛋白
实验模型和无对照的病例研究:静脉免疫球蛋白(IVIG)显示有抗病毒和免疫调节效应,提示其在心肌炎中可能有治疗用途。
心肌炎和急性心肌病干预临床试验: 接受IVIG治疗的急性扩张型心肌病患者(的转归)并不好于接受安慰剂者。
缺乏病毒性或自身免疫性、活检确诊心肌炎的多中心随机研究,并不推荐在成人中常规使用IVIG 治疗急性心肌炎。
IVIG无明显副作用,可用于传统抗心衰治疗抵抗的心肌炎,病毒性和自身免疫性心肌炎,尤其是自身抗体介导者。
远期预后[4]
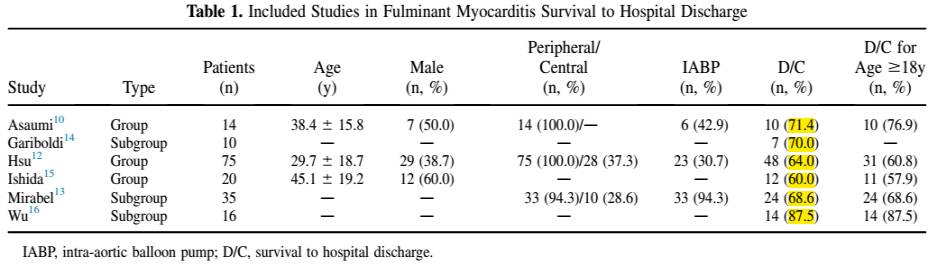
1 年生存率:暴发性心肌炎 93% ,急性淋巴细胞性心肌炎85%
11年生存率:93% 比45%
1、Pollack,A.et al.Nat.Rev.Cardiol.advance online publication 21 July 2015;
2、2013 ESC心肌心包疾病专家共识
3、Curr Heart Fail Rep (2014) 11:166–177
4、N Engl J Med 2000;342:693;