


根据ESC/HFSA/AHA/ACC心衰指南,HFpEF=心衰症状或体征+EF≥50% + LV大小正常,排除明显的瓣膜病、心包疾病、先心病、高输出型心衰、肥厚型心肌病等。
洪教授强调,左室舒张功能的紊乱,仍然是HFPEF确诊的重要标准。
HFPEF机制不清,有心血管和非心血管等多种机制参与。 因此,如果存在下列情况,目前的指南也支持HFPEF的诊断:临床表现持续存在,舒张功能紊乱不明确,但有其他证据支持HFPEF相关不良的心血管重构(左室增厚,左房增大,心房纤颤)。当然HFPEF的诊断标准将会伴随着对它的认识而不断修正。
不均一性临床综合征:多种病因+共病
缺乏有效的治疗方法
发病率逐渐增加,死亡率也增加
老年、女性多
共病多(心脏+非心脏疾病)
发病机制尚未完全清楚
舒张功能失调(DD)、舒张性心衰(DHF)和 HFpEF区别
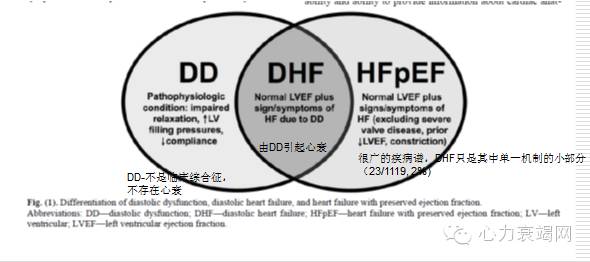
诊断标准:共识为基础的诊断标准,临床研究和实验证明HFpEF是呈现异质性的临床综合征。
动物实验:缺乏能真正代表HFpEF的动物模型,动物模型通常仅聚焦于1或2个HFPEF的特征如主动脉结扎、高血压、肥胖、糖尿病、肾脏疾病、老化或非梗死性缺血性心脏病。
人体试验:有限,尤其缺乏直接人心肌的资料分析。
发病机制:已经提出多种发病机制,但停留在假说上 。
存在共病:HFpEF常患有高血压、糖尿病、血管病、肾病、房颤和代谢综合征、COPD、贫血、睡眠呼吸障碍等共病,而这些共病HFpEF的临床表现及其结局(包括死亡)产生重要的影响。
认识的转变:
“cardio-centric” model
左室舒张功能失调
(以疾病和病变为中心)
▼
multiple cardiovascular
and noncardiovascular mechanisms
多种心血管和非心血管机制
(以病人为中心)
HFpEF整体的病理生理
LV肥厚
LV舒张功能松弛缓慢,左室舒张硬度增加
LV收缩性能下降,收缩功能储备下降
冠脉血管:CAD、冠脉微血管病
心血管结构异常
左房:结构重构、增大,其程度可反映HFpEF的严重性和病程。
压力负荷重构:左房压力增加,右室负荷增加,大“V”波,HFpEF的血液动力学特征。
电重构:房颤,恶性循环
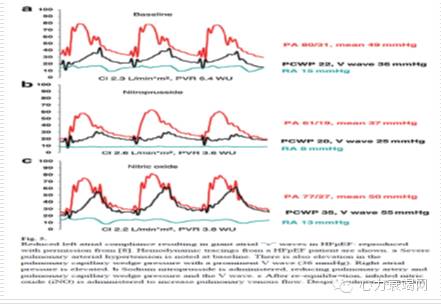
HFpEF左房顺应性下降导致大“V”波
肺血管和右室:HFpEF的肺静脉高压,肺动脉高压,RV负荷增加,右室功能障碍;肺动脉高压可以反映HFpEF的病情严重性及其结局。
心室相互作用增强: 心包与外部因素占休息状态下的左室舒张末期压力的1/3。HFpEF左房和右室明显增大,可加大心室间的相互作用,在发病过程中起重要作用。
心血管功能异常
变时功能下降(心率反应性下降,Chronotropic incompetence): 50-75%HFpEF患者有变时功能下降(不依赖于负性频率药物),原因:β受体下调导致全身自主功能失调。
储备功能下降:HFpEF患者的主要特征:活动耐力下降。”早期储备功能下降“是HFpEF的首要表现(变时功能、周围血管扩张、LV舒张、左室收缩、心室血管偶联等储备功能下降 )
心肌结构和功能变化——心肌生物学
资料有限,心内膜活检、外科手术标本少
心肌硬化:HFpEF患者心肌硬化高, 心肌纤维化
NO信号传导障碍:cGMP下降、PKG活性下降,而心肌NO氧化水平提高;
Titin(肌联蛋白)结构和功能变化:肌联蛋白---分子弹簧作用
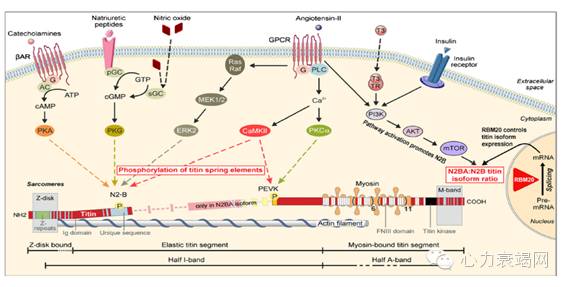
Titin的结构和功能变化
HFpEF的病理生理学特点可归结为:心肌肥厚性重构和RASS的激活以及多病共存。关于多病共存,有人认为:HFpEF仅仅是共病各个体对心血管结构和功能作用的顶峰表现。但是,共病+HFpEF,比无HFpEF,心血管结构和功能异常多,结局差。而且,共病+HFpEF与相同年龄、相同性别共病无HFpEF之间区别尚未阐明。
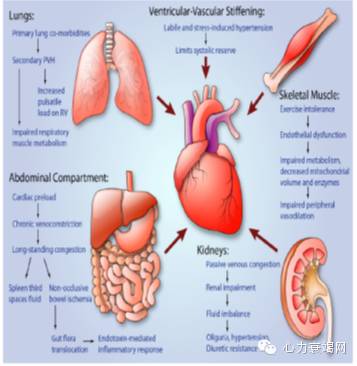
HFpEF新的理念—内皮功能障碍
共病导致全身炎症反应,增加氧化应激与广泛血管内皮功能障碍。在心肌水平方面,存在冠脉微血管内皮炎症和功能障碍和心脏内皮--心肌细胞信号传导失调,最终引起心肌细胞和细胞外基质出现明显结构和功能的改变。
心肌以外的全身各部位血管床的内皮功能障碍构成的血管舒缩功能障碍,导致心室--血管偶联异常、肺动脉高血压、肾功能不全,和运动耐量下降。
非心脏方面的发病机制
周围骨骼肌代谢改变
肺动脉高压
肾功能不全
腹部,肠道菌群
骨骼肌:
HFpEF:VO2峰值下降。Kitzman研究显示:HFpEF患者股外肌I氧化肌肉纤维减少,I/II纤维比值,毛细血管/纤维比值下降,II型纤维增加,上述变化与VO2下降明显相关;运动耐力下降与内皮功能损害和异常平滑肌代谢有关:包括线粒体体积、酶学和肌肉萎缩等。另外还跟心力衰竭所致的衰弱有关。
肾功能下降:
发生率高,26-53%,机制尚未清楚,目前有以下几种推测:共病导致肾本身内在的损伤, RASS的激活、静脉淤血,药物的损害,最终引起心脏的炎症、纤维化 ---HFpEF
腹部的作用:
HFpEF患者,周围浮肿较少,但腹水发生率相对较高,为什么?我们推测腹部可能在心肾综合征中起重要作用。正常情况下,内脏容量血管能储存25%的总血容量,HFpEF时,这储备功能减少,神经内分泌激活,静脉收缩,毛细血管静水压增加,导致富有蛋白质的浮肿和第三间隙扩大。当毛细血管静水压>腹腔内压≥2mmHg(5-7,N),将引起下列异常: 肝调节肾功能、内脏血管床淤血导致假性低血容量状态、非梗阻性肠道缺血、循环内毒素增加,炎症。
肠道菌群失调,肠道菌群代谢产物改变
病理生理分型
临床/病因学分型
基于临床表现的分型
表型组学分型
专家简介
洪华山,男,主任医师,医学博士、教授、博士生导师、主任医师,留学博士后,协和医院副院长,干部病房行政主任。为福建省优秀专家、国务院特殊津贴专家。省“百千万人才工程”人选,是省青年科技奖获得者,中华医学会福建省心血管分会常委,为《中华高血压杂志》和《中国临床药理学和治疗学》编委。曾获得省部级科技进步奖6项。擅长心血管疑难急危重病诊治,尤其在心力衰竭、高血压的诊治方面有丰富的经验。