


在2017中国国际心力衰竭大会(CIHFC)暨中国医师协会心力衰竭专业委员会年会上,来自宾夕法尼亚大学的Kenneth B. Margulies教授为我们带来了“慢性心衰转变为急性失代偿的细胞改变 ”的精彩报告。

免责声明
与急性心衰失代偿相关的最常见情况并非从细胞水平开始
♦缺血
♦急性容量/后负荷增加→室壁张力增加,房室瓣膜反流
♦超过心脏储备的系统生理需要
♦系统性炎症反应
♦心肌毒性
……然而这些因素能刺激心肌细胞的变化。
收缩功能储备
♦什么是收缩功能储备?
——心脏在应对短期生理负荷时增加收缩功能的能力
♦增加收缩功能的机制?
——前负荷增加(Frank-Starling机制)
——心率增快(力-频效应)
——β– 肾上腺素能刺激
人心肌细胞长度和主动张力的关系
[1]
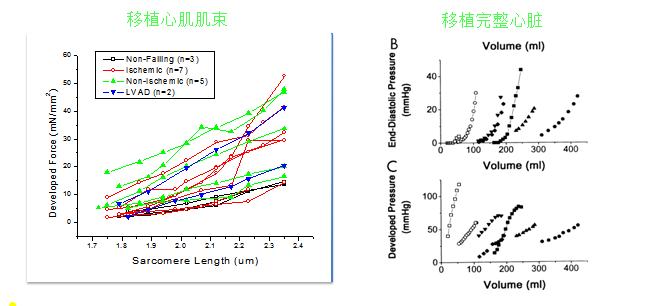
♦前负荷和张力增加存在正相关关系
♦尽管被动/舒张性僵硬度增加常出现在患病心脏,在衰竭心脏和非衰竭心脏中前负荷相关储备似乎均完好。
功能不全的心脏中力-频关系受损
[2]
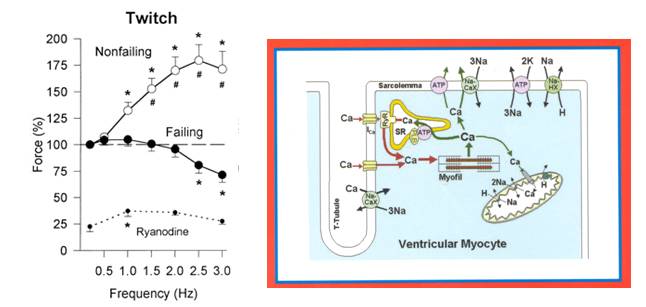
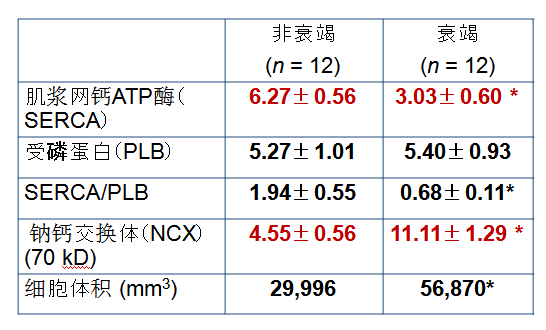
钙调蛋白在非衰竭和衰竭心脏中的浓度
[3]
衰竭心脏中β肾上腺素能反应受损
[4]
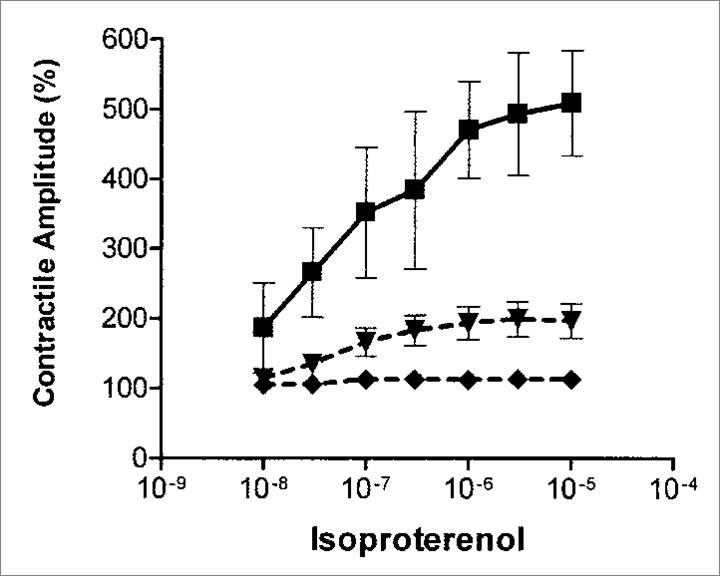
β肾上腺素能对收缩功能调控依赖于钙离子循环的变化
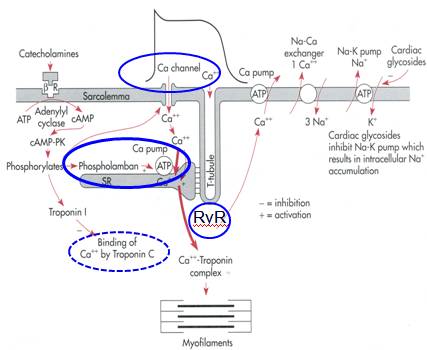
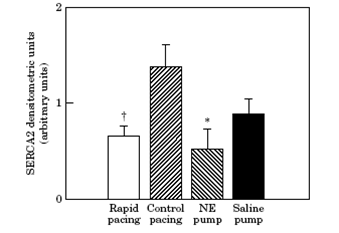
外源性儿茶酚胺模拟心衰中下调的SERCA表达
心肌收缩功能储备总结
♦在严重衰竭心脏中,Frank-Starling机制完好,但心率和肾上腺素能依赖性收缩功能储备严重下降
♦心肌细胞钙循环障碍,部分原因是钙调节蛋白浓度的变化。它是收缩功能下降的主要原因。
♦β肾上腺素能刺激可以加剧SERCA基因表达的病理性下调
代偿性扩张型心肌病中心肌细胞的脂肪酸和葡萄糖代谢
[6]
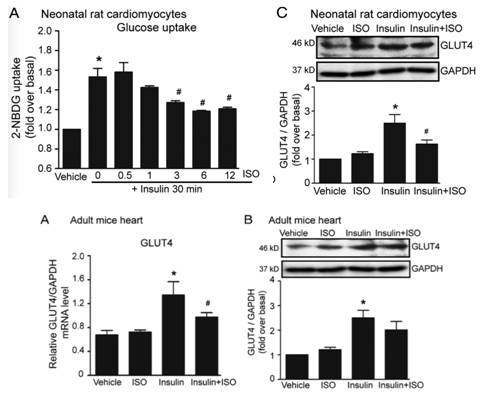
β肾上腺素能对心肌细胞胰岛素敏感性的刺激作用
[7]
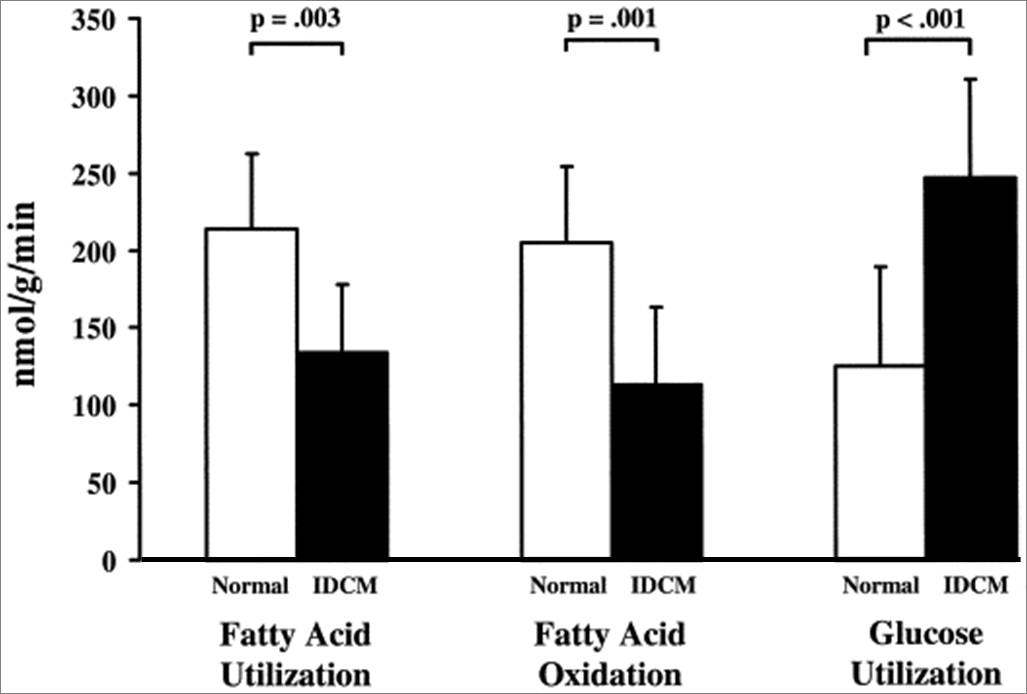
进展性心衰的代谢底物利用(犬快速起搏模型)
[8]
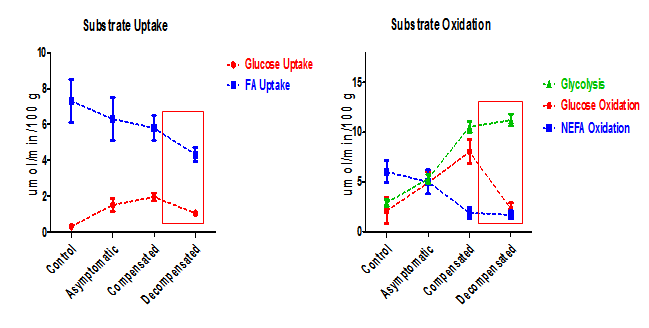
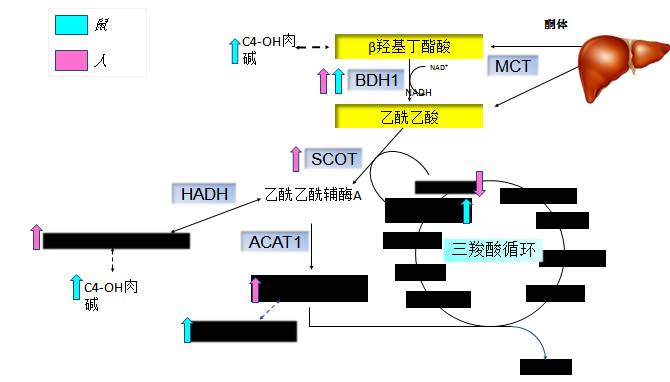
在鼠和人心衰中酮体氧化增加的代谢证据
[9]
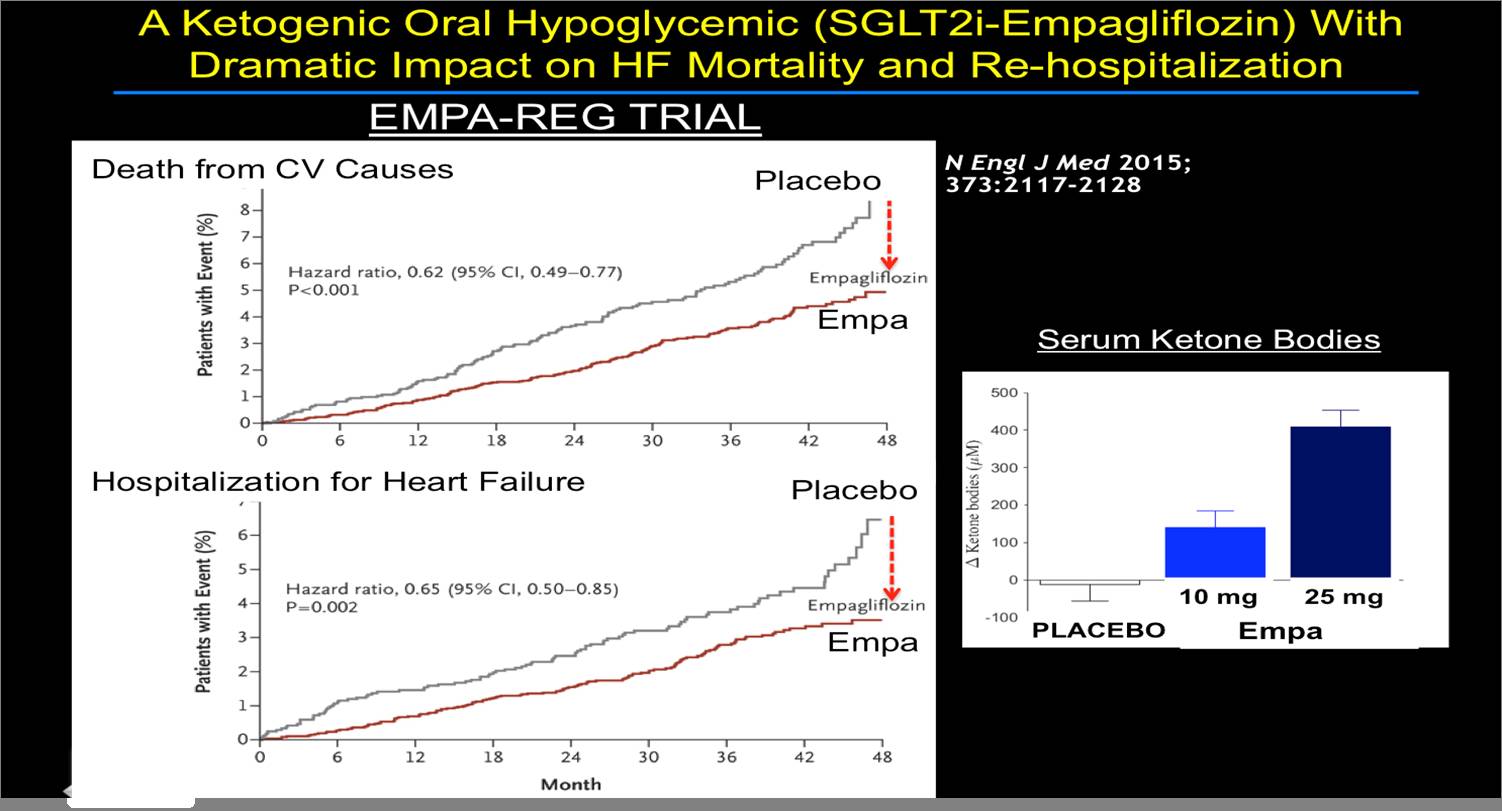
生酮口服降糖药(钠-葡萄糖协同转运体2抑制剂SGLT2i-Empagligozin)对心衰死亡率和再住院率的戏剧性作用
心肌代谢总结
♦在严重衰竭心脏,由于葡萄糖利用代偿性上调,脂肪酸代谢下降
♦β肾上腺素能刺激减少心肌胰岛素抵抗以适应代偿性增加的葡萄糖利用
♦近期来自移植心脏组织和临床试验的证据提示,酮体利用增加可能是进展性心衰代谢代偿的一部分。
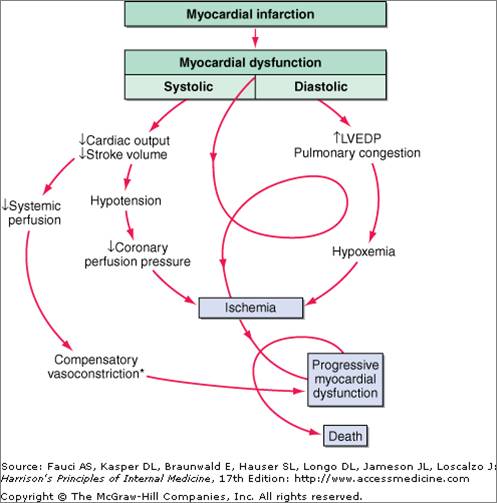
心源性休克的病理生理学
心肌细胞长度和主动张力的关系
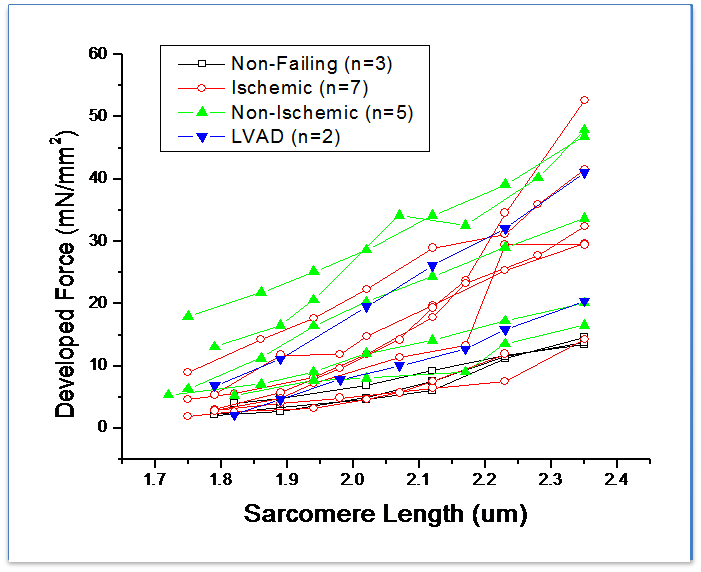
♦前负荷和张力增加之间存在正相关关系
♦尽管在病变心脏中被动张力/舒张性僵硬常常增加,衰竭心脏和非衰竭心脏中前负荷依赖性心脏储备均保留
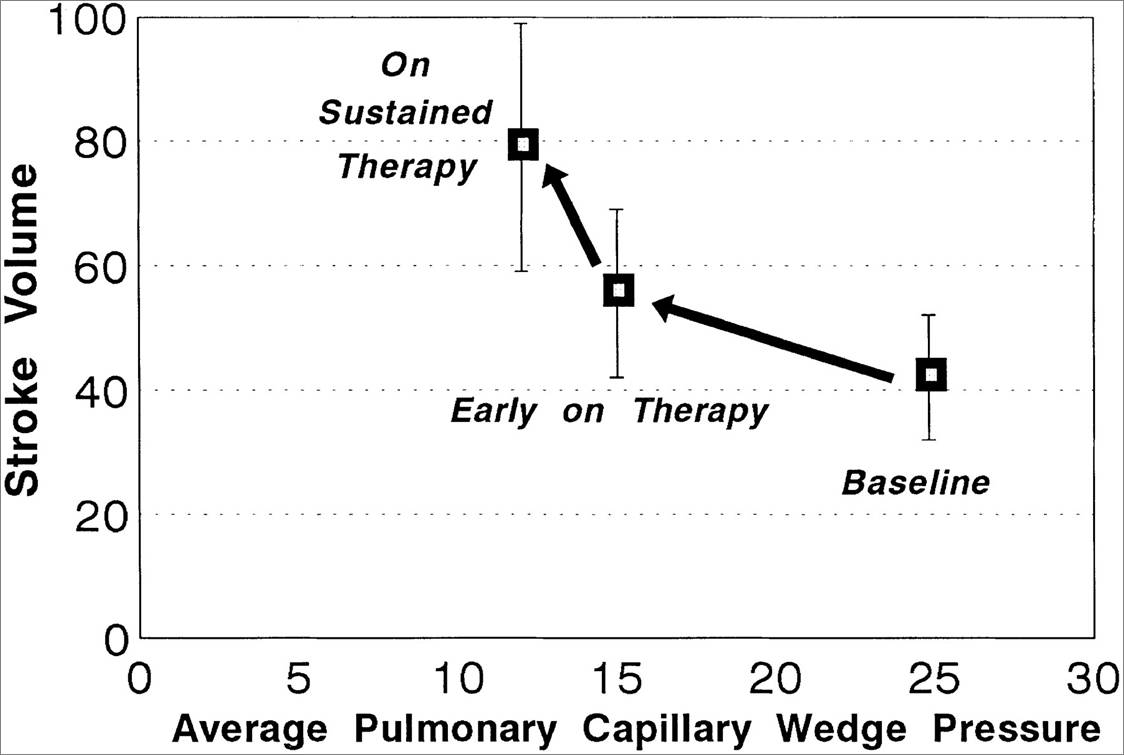
基线水平、初始治疗24-72小时后,治疗8个月后肺毛细血管楔压和每搏输出量的关系
[10]
微管参与心肌细胞伸展传感
[11]
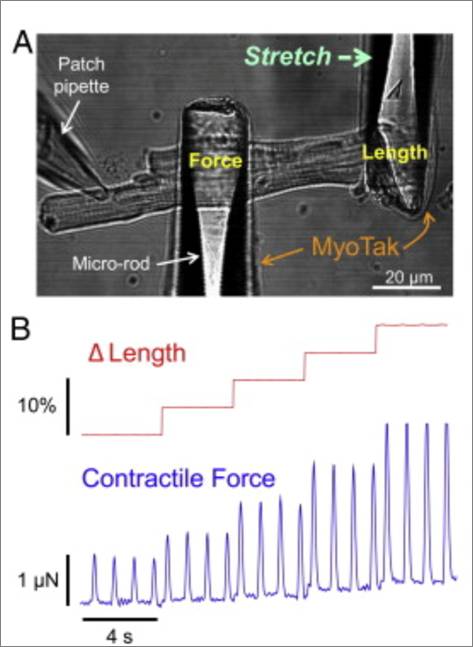
A. 心肌细胞借助MyoTak-coated rods附着和伸展
B. 以1Hz的频率用相同收缩力刺激心室肌细胞,心肌细胞长度逐步变化(5-20%)
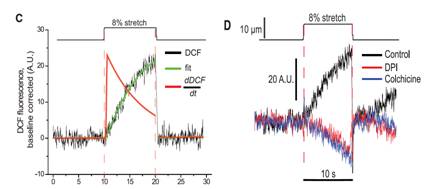
伸展产生细胞内氧化应激信号
C. DCF荧光信号标记出氧化应激反应在心室肌细胞伸展时产生8%。在伸展时氧化应激反应有迅速和短暂的增长。
D. NAFPH氧化酶2的特异性抑制剂或秋水仙碱致微管破裂可以阻断伸展后细胞内氧化应激反应产生
Stretch→ microtubule sensing → NOX2 ? ROS
氧化酪蛋白受抑制时微管弯曲减少
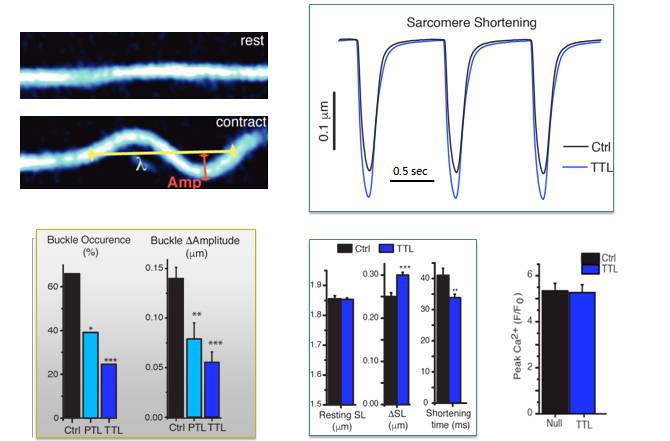
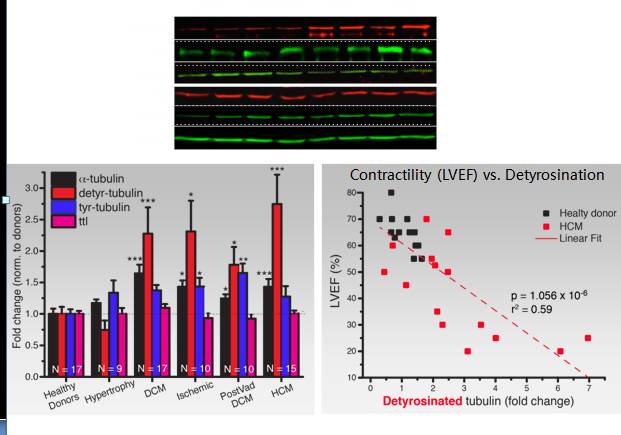
微管去酪氨酸化与衰竭心脏功能不全相关
[12]
Summary & Conclusions总结和结论
♦ 心肌病理状态下的心脏收缩功能储备减少,SERCA 2a下调,产生ATP的主要底物由脂肪酸变为葡萄糖
♦急性生理应激伴随内源性和外源性儿茶酚胺增加进一步减少SERCA的表达,同时抑制葡萄糖摄取
♦心肌细胞伸展的急性增加刺激微管依赖性氧化应激信号和增加微管去酪氨酸化,从而进一步损害肌细胞收缩力
♦治疗策略包含早期机械循环支持以限制儿茶酚胺应激和心脏扩大,或靶向治疗,如直接SERCA激动剂,选择性代谢底物或利于微管酪氨酸化的制剂
UPenn
Ben Prosser
Patrick Robison
Matt Caporizzo
J Eduardo Rame
Ken Bedi
Temple
Steve Houser
Eric Rossman
Khouram Chaudhary
Sanford Burnham Institute
Dan Kelly
Greg Aubert
Ola Martin
Julie Horton
Rick Vega
Ling Lai
细胞凋亡通路
[13]
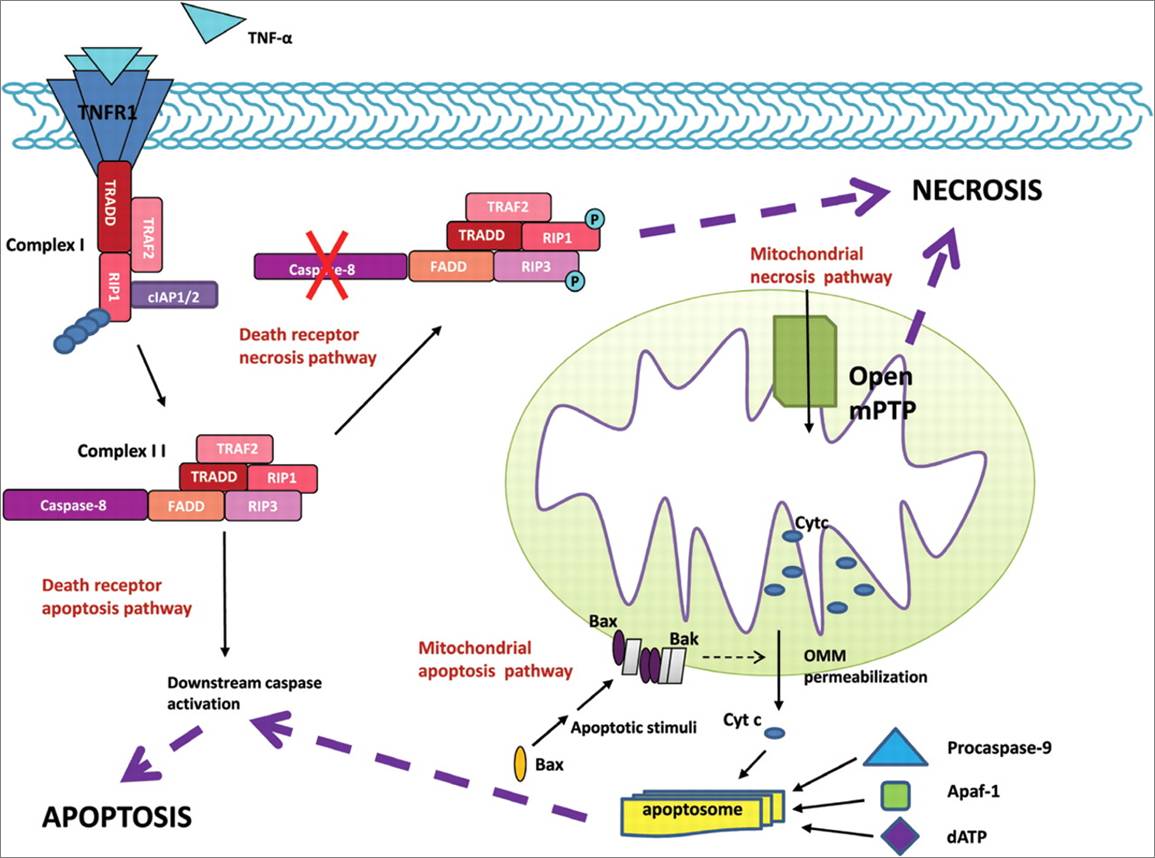
[1]Holubarsch C, et al. Circulation 1996; 94:683-689.
[2]Pieske B. Circ Res 1999;
85:38-46.
Bers D. Excitation-Contraction Coupling and Cardiac Contractile Force.
Springer, Netherlands, 2001
[3]Chaudhary KW et al, J Am Coll Cardiol. 2004; 44:837-45
[4]Moniotte S. Circulation 2001; 103(12):1649-55.
[5]Lai et al. J Mol Cell Cardiol 1998; 30:175-85
[6]Dávila-Román VG, et al. J Am Coll Cardiol 2002; 40:271–277
[7]Mangmool S, et al. Molecular Endocrinology 2016, 30,118-132
[8]Nikolaidis LA, et al. Cardiovasc Res. 2004; 61:297-306
[9]Aubert et al; Bedi et al Circulation. Feb, 2016;
Nature Rev. Cardiol.. March, 2016
[10]Steimle AE et al. Circulation. 1997;96:1165-1172
[11]Prosser B et al. Science 333:1440-5, 2011
[12]Robison P…Prosser BL Science 352 (6284): 2016
[13]Konstantinidis K et al. ATVB 2012;32:1552-1562
专家简介

Kenneth B. Margulies,MD is Research Director, Heart Failure/Transplantation, Professor of Medicine at the Hospital of the University ofPennsylvania and Professor of Physiology. Dr. Margulies is a member of AmericanCollege of Cardiology, American Federation for Clinical Research, AmericanHeart Association, American Society of Clinical Investigation, Committee onAcademic Freedom and Responsibility, Heart Failure Society of America, InternationalSociety of Heart and Lung, Transplantation, National Institutes of Health. Dr.Margulies’s specialty interest is in Advanced Heart Failure and TransplantCardiology. The focus of his research include Integrative Genomics of HumanHeart, Engineered Cardiac Microtissues, Myocardial Metabolism in Heart Failureand Endogenous Cardiac Repair. He has published over 100 manuscripts in medicaland scientific journals suc。