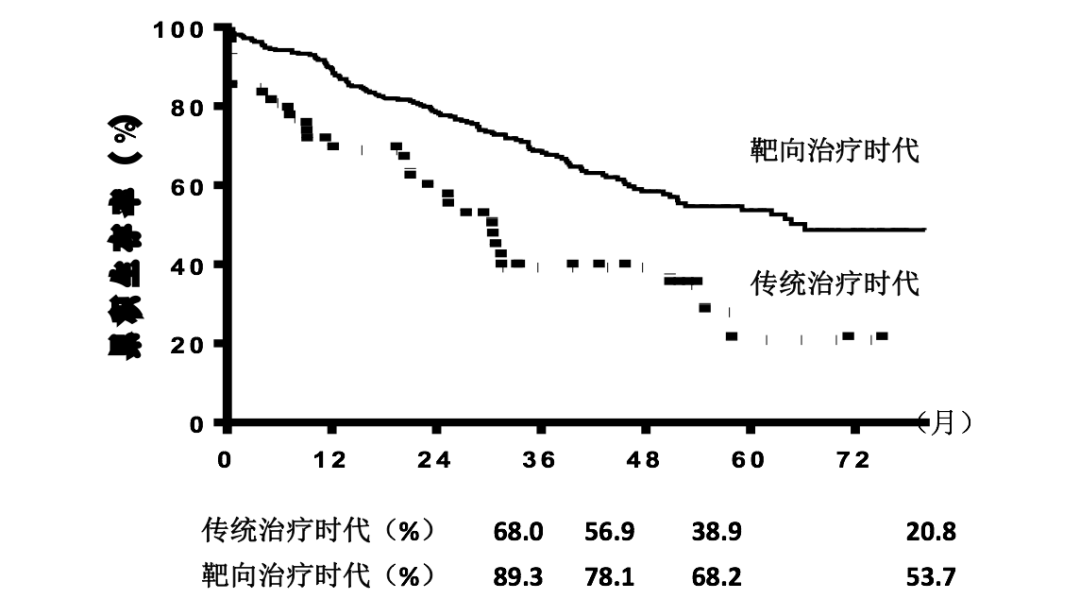
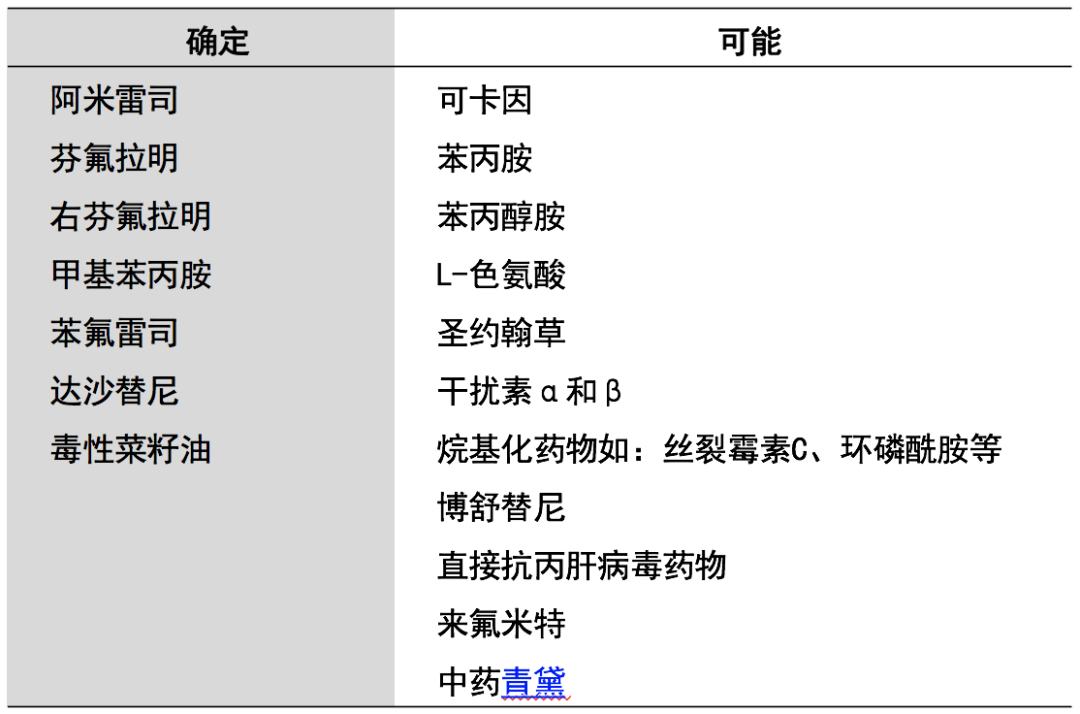
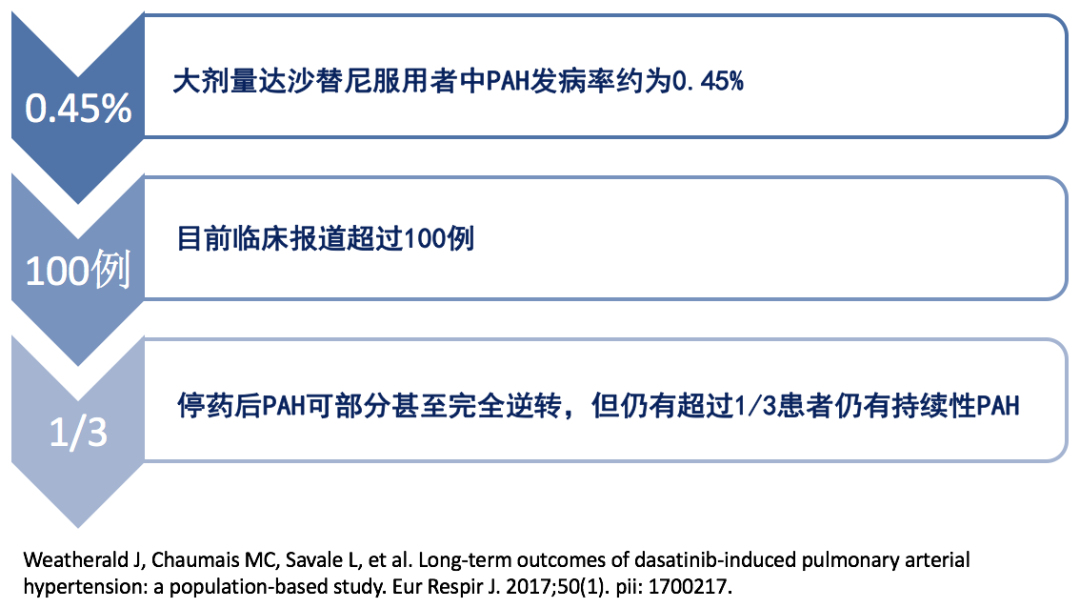
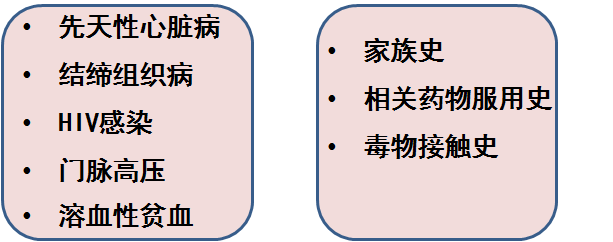
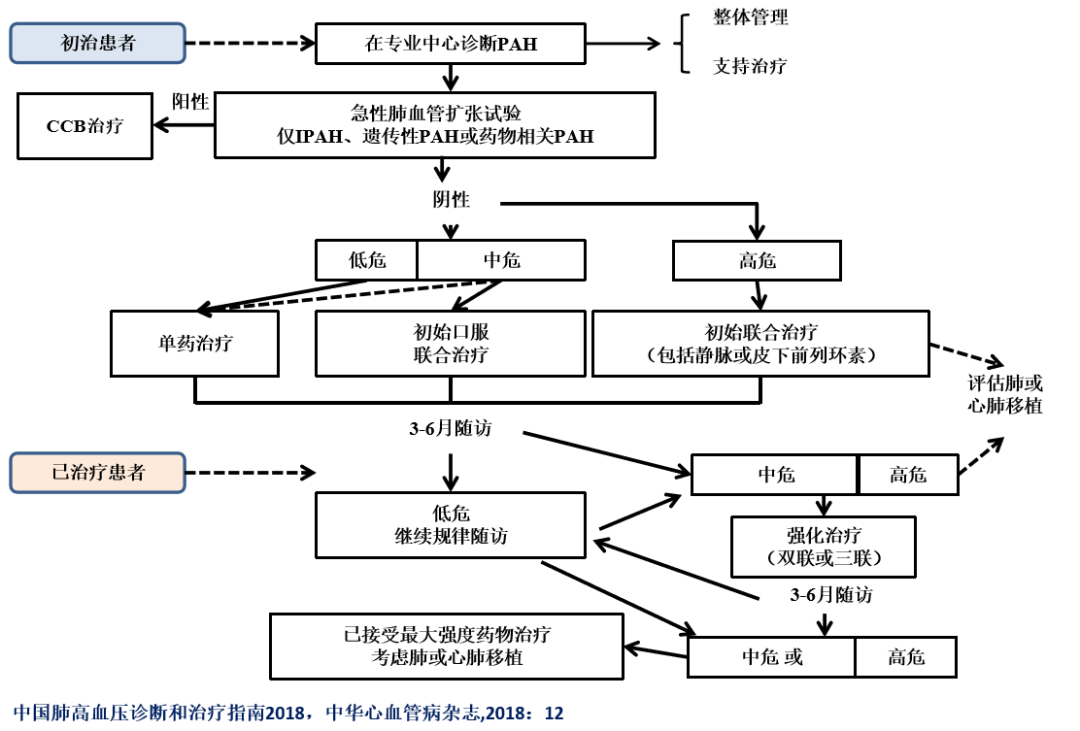
▲ 中华医学会心血管病学分会、中华心血管病杂志编辑委员会联合发布我国“肺动脉高压筛查诊断与治疗专家共识” (2007年7月)
▲ 该共识参考第3届世界肺高血压大会进展(2003年),结合我国实际制定
▲ 规范临床医生的诊疗行为、提高我国肺高血压临床诊治水平发挥重要作用
— CTPEH治疗进展取得重大突破(外科、介入和药物治疗)
— 第4-6届WSPH及ESC/ERS指南公布
▲ 我国在该领域研究工作进展亦相当迅速,有必要对我国共识进行修订和更新
— Ⅰ类:指已证实和/或一致公认有益、有用和有效的操作或治疗
— Ⅱ类:指有用和/或有效的证据尚有矛盾或存在不同观点的操作或治疗
— Ⅱa类:有关证据/观点倾向于有用和/或有效,应用这些操作或治疗是合理的
— Ⅱb类:有关证据/观点尚不能被充分证明有用和/或有效,可考虑应用
— Ⅲ类:指已证实和/或一致公认无用和/或无效,并对一些病例可能有害的操作或治疗,不推荐使用
— 证据水平A:资料来源于多项随机临床试验或荟萃分析
— 证据水平B:资料来源于单项随机临床试验或多项非随机对照研究
— 证据水平C:仅为专家共识意见和/或小型临床试验、回顾性研究或注册登记
▲ 肺高血压:pulmonary hypertension
▲ 肺动脉高压:pulmonary arterial hypertension
▲ 特发性肺动脉高压:idiopathic pulmonary arterial hypertension
▲ 本指南仍保持与2007年“肺动脉高压筛查诊断与治疗专家共识”一致,原因如下
— 我国学术界习惯将“pulmonary embolism” 译为“肺栓塞”而不是常规译为 “肺动脉栓塞”,几乎没有学者认为“肺栓塞”还包括“支气管动脉栓塞”或“支气管、肺泡内部堵塞”等引人异议的理解
— 日本、台湾学者也均将“pulmonary hypertension”翻译为“肺高血压症”
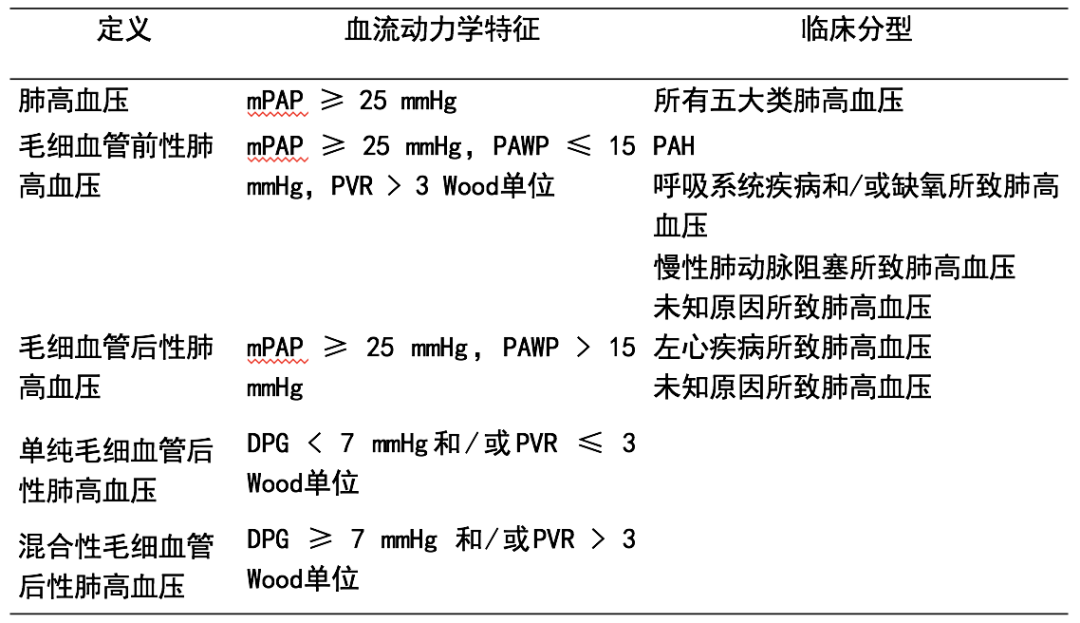
— 是一个血流动力学概念,指右心导管测量肺动脉平均压(mPAP)≥25mmHg
— 根据血流动力学特点不同,肺高血压可分为毛细血管前和毛细血管后两大类
— 是一类以肺血管阻力进行性升高为主要特点的恶性肺血管疾病,可导致右心衰竭甚至死亡
— 诊断标准:海平面状态,静息时右心导管检查肺动脉平均压(mPAP) ≥25mmHg,同时肺毛细血管嵌顿压(PCWP)≤15 mmHg,肺血管阻力>3 WU
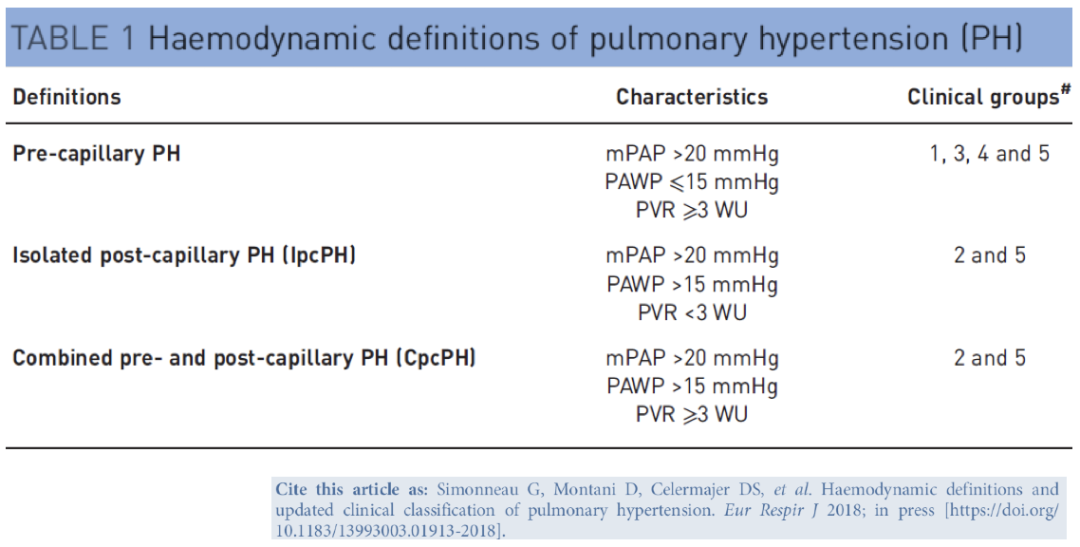
Haemodynamic definitions of PH: 6th WSPH
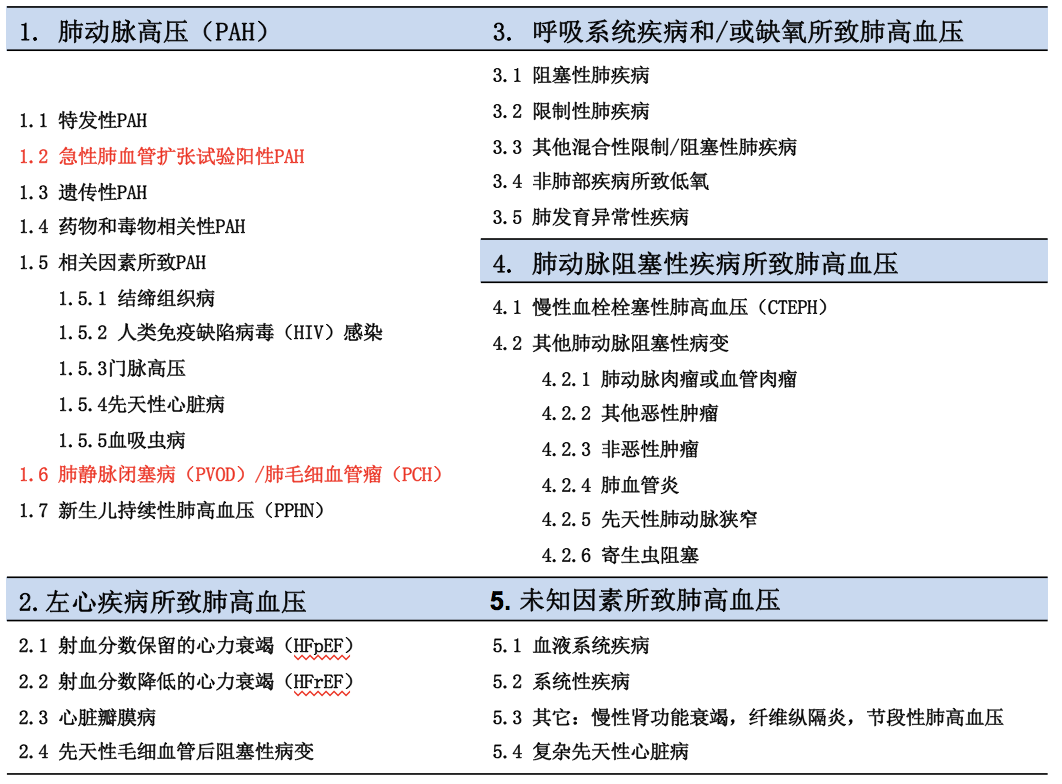
▲ 急性肺血管扩张试验长期阳性肺动脉高压患者对大剂量钙通道阻滞剂敏感,预后良好,且有特异治疗方案

▲ 当前研究发现PVOD/PCH主要与EIF2AK4双等位基因突变有关,并且合并肺静脉和肺毛细血管受累的征象

▲ 普通人群中肺高血压患病率约为1%,>65 岁人群高达10%,以左心疾病、呼吸系统疾病和/或缺氧所致肺高血压最常见
▲ 普通人群中PAH发病率和患病率分别为5~10/百万人年和15~60/百万,约半数为IPAH、遗传性PAH 或药物相关PAH
▲ 相关因素PAH以结缔组织病最常见,其中系统性硬化症约占2/3
▲ 近年来IPAH平均诊断年龄为50~65岁,较20世纪80年代的36岁显著增大,原因尚不明确
▲ 最常见的PAH病因为先天性心脏病,其次为IPAH和结缔组织病相关PAH
▲ 结缔组织病相关PAH最常见为系统性红斑狼疮和干燥综合征
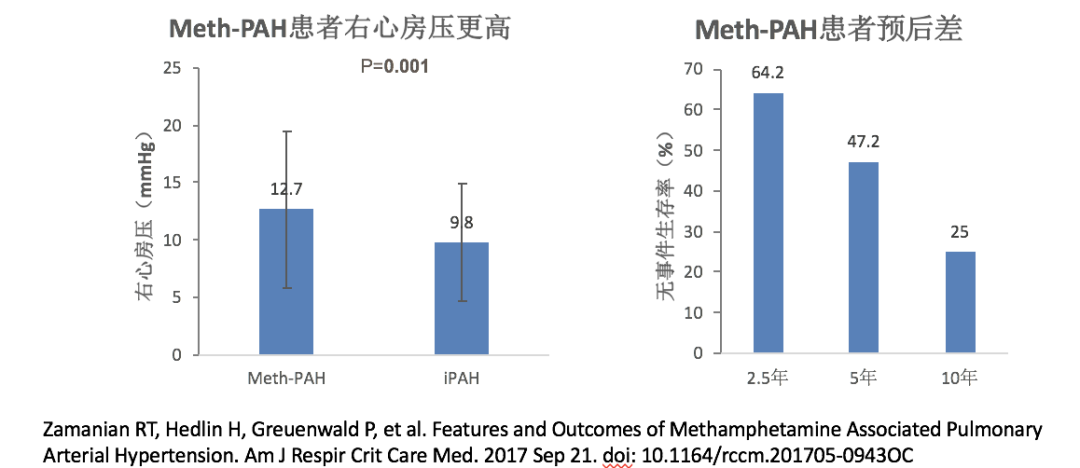
▲ 注册登记研究中甲基苯丙胺相关PAH患者数量与IPAH相当,患病率远远高于一般人群
▲ 甲基苯丙胺相关PAH患者心衰症状更严重,预后也比IPAH更差
— BMPR2、BMP9、ACVRL1、ENG、SMAD9、BMPR1B、TBX4、CAV1和KCNK3
— 可解释50%~80%的遗传性PAH和20%~50%的IPAH的病因
— 最新发现的PAH致病基因,使发病风险上升22倍,可解释6.7%中国IPAH患者的遗传病因
▲ 病理改变包括肺动脉中膜肥厚、内膜增殖和纤维化、外膜增厚纤维化等,严重病变包括丛样病变、扩张型病变等复合病变
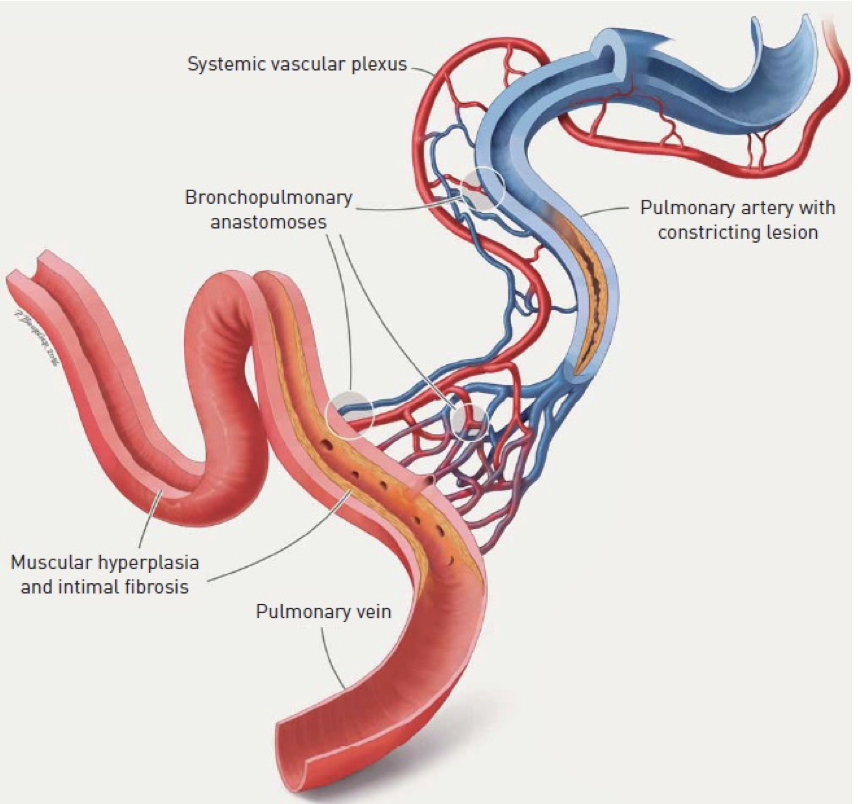
▲ 所有类型肺高血压除肺动脉重构外,肺静脉甚至肺毛细血管也可发生重构或增殖性改变
— 支气管血管丛与肺静脉吻合支大量开放,肺静脉血流增加
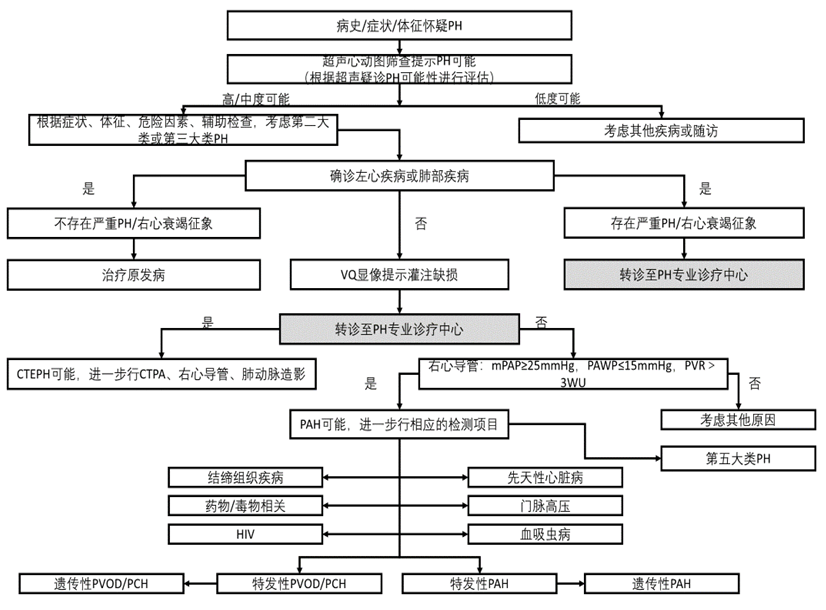
▲ 加强肺高血压诊断意识,对疑诊患者应详细询问肺高血压相关症状及诱发因素,收集既往疾病史、家族史、生育史、减肥药或毒物接触史及高原居住史等,并完善体格检查[Ⅰ,C]
▲ 临床疑诊肺高血压的患者,应完善实验室检查[血常规、电解质、转氨酶、胆红素、肌酐、尿酸、D-二聚体、B型利钠肽(BNP)或N末端B型利钠肽原(NT-proBNP)、甲状腺功能及动脉血气分析等],综合评估病情[Ⅰ,C]
▲ 临床疑诊肺高血压的患者,应常规进行心电图、胸部X线平片、超声心动图、呼吸功能、CT肺动脉造影、肺通气灌注显像、心肺运动试验等检查,尽早完善右心导管检查,进行准确诊断分类[Ⅰ,C]
▲ 肺动脉高压患者应常规检测BNP和NT-proBNP,治疗过程中尽量维持正常或接近正常范围
— 其他支持征象包括RV/LV基部内径>1、室间隔变平或左移、PA内径>25 mm、下腔静脉内径>21 mm及吸气时塌陷率<50%等
▲ 发现心内结构、功能异常或血管畸形等:先天性心脏病、左心疾病等
▲ 右心功能评估:通过右房大小、三尖瓣环收缩期位移(TAPSE)、Tei指数以及有无心包积液等间接评价
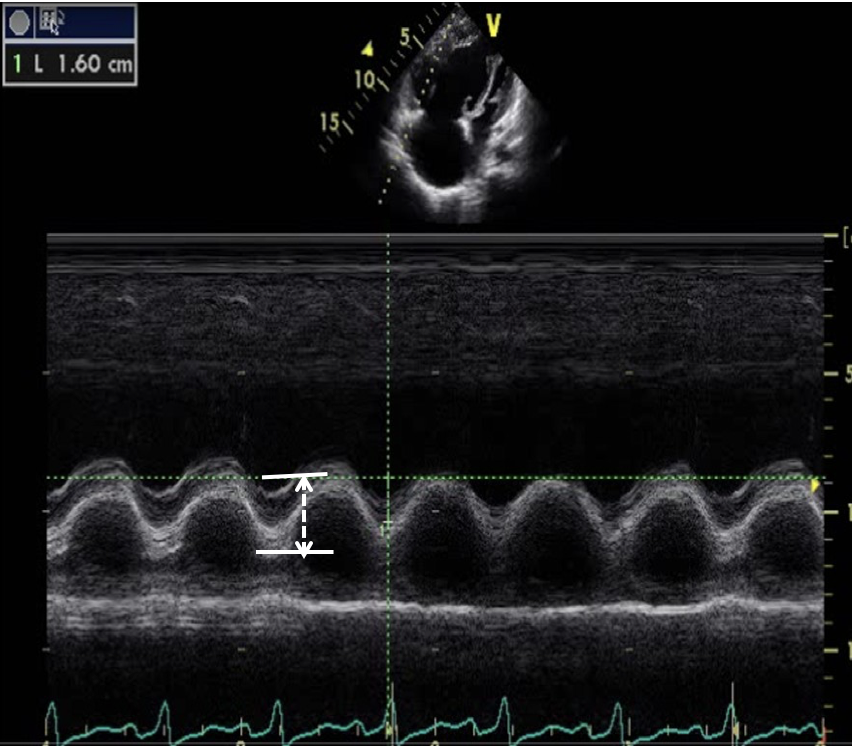
— 相当比例患者估测PASP和右心导管测定sPAP相差20mmHg以上,部分甚至达到40mmHg以上Rich JD, et al. CHEST. 2011

▲ 三尖瓣峰反流速度≤2.8m/s,无其他肺高血压征象,则肺高血压可能性低,建议定期复查超声心动图(Ⅱa,C)
▲ 三尖瓣峰反流速度≤2.8m/s,有其他肺高血压征象,或三尖瓣峰反流速度2.9~3.4 m/s,无其他肺高血压征象,则肺高血压中度可能,建议进一步检查包括右心导管检查(Ⅱa,C)
▲ 三尖瓣峰反流速度2.9~3.4m/s,有其他肺高血压征象,或三尖瓣峰反流速度≥3.4 m/s,无论有无其他肺高血压征象,则肺高血压高度可能,建议进一步检查包括右心导管检查(Ⅰ,C)
▲ V/Q显像不匹配提示PE,CTEPH或Takayasu大动脉炎等疾病
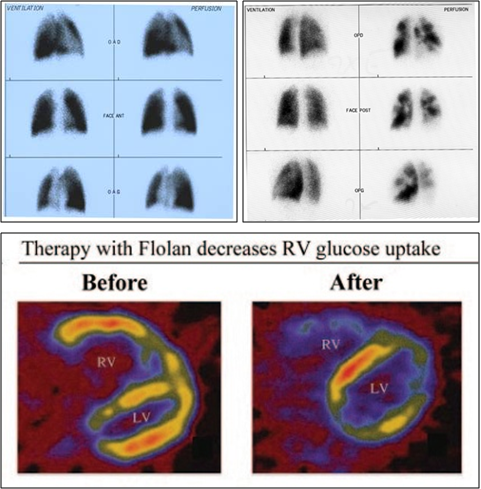
▲ 不仅是确诊肺动脉高压的金标准,也是指导制定科学治疗方案必不可少的手段
▲ 在有经验的肺血管病诊治中心,右心导管检查并发症发生率仅为1.1%,死亡率更低于0.055%
▲ 对分流性先心病心排血量计算应采用Fick法,对无心内外分流患者心排血量的测量应采用温度稀释法
— 测定“心室平均压”而非心室舒张末压(LVEDP or RVEDP)
— 穿刺路径:使用Swan-Ganz导管避免股静脉入路
— 导丝:Swan-Ganz导管需配备0.025″导丝
▲ 右心导管检查是确诊肺高血压、诊断分类及治疗指导的重要检查手段(Ⅰ,C)
▲ 建议患者转诊到肺血管疾病区域医疗中心进行右心导管检查,检查结果更全面,安全性更高(Ⅰ,B)
▲ 评估肺高血压疗效可进行右心导管检查(Ⅱa,C)
▲ 评估先天性心脏病是否适合介入封堵或手术修补需进行右心导管检查(Ⅰ,C)
▲ 左心疾病或呼吸系统疾病所致肺高血压拟器官移植前需进行右心导管检查(Ⅰ,C)
▲ 右心导管检查无法获得PAWP,可测量左心室舒张末压代替(Ⅱa,C)
▲ 疑诊左心疾病或呼吸系统疾病所致肺高血压时应进行右心导管检查,以明确诊断和指导治疗(Ⅱb,C)
▲ CTEPH患者应进行右心导管检查明确诊断及指导治疗(Ⅰ,C)
▲ 部分特发性PAH、遗传性PAH或药物相关PAH的发病机制可能与肺血管痉挛有关,急性肺血管扩张试验是筛选这些患者的有效手段
▲ 急性肺血管扩张试验阳性提示肺循环内有相当多的肺小动脉处于痉挛状态,采用钙通道阻滞剂治疗可显著改善试验结果阳性患者的预后
▲ 特发性PAH、遗传性PAH或药物相关PAH患者首次行右心导管检查时,必须同时行急性肺血管扩张试验
▲ 国际推荐使用一氧化氮(10-20 ppm)、静脉注射依前列醇、腺苷或伊洛前列素

▲ 超声心动图是疑诊肺高血压时一线无创诊断方法(Ⅰ,C)
▲ 无法解释肺高血压需排除CTEPH时建议进行肺灌注或肺通气灌注显像检查(Ⅰ,C)
▲ 疑诊CTEPH时建议进行CT肺动脉造影检查(Ⅰ,C)
▲ 所有肺高血压患者均应进行血常规、血生化、自身免疫抗体、HIV抗体、甲状腺功能检查(Ⅰ,C)
▲ PAH考虑门脉高压引起时建议进行腹部超声检查(Ⅰ,C)
▲ 肺高血压首次评估时建议完善呼吸功能包括DLco检查(Ⅰ,C)
▲ 所有肺高血压患者均应完善高分辨肺CT检查(Ⅱa,C)
▲ CTEPH患者应进行肺动脉造影检查(Ⅱa,C)
▲ 不建议对肺高血压患者进行开胸或胸腔镜肺活检(Ⅲ,C)
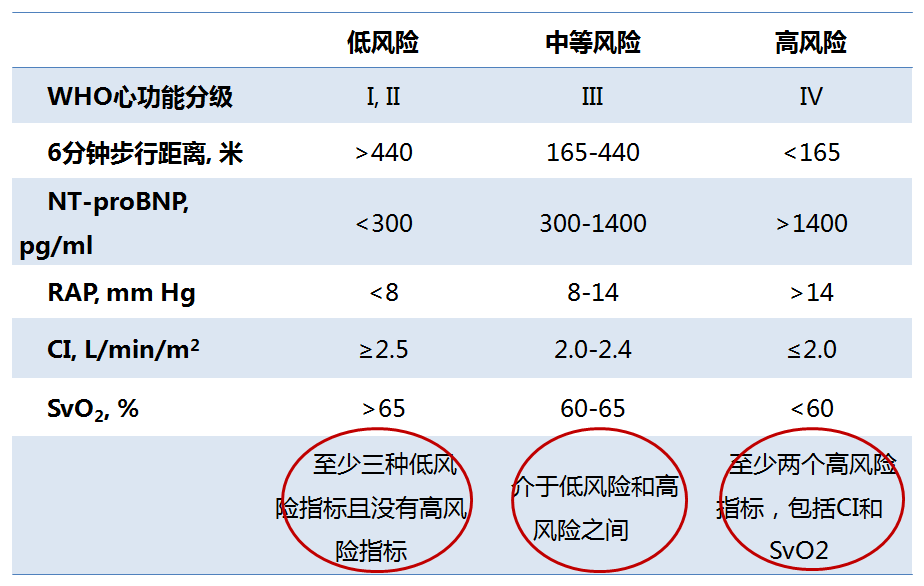
▲ WHO心功能分级:强调晕厥症状的重要性,与预后密切相关
▲ 心肺运动试验:评价肺高血压患者运动功能受损、药物疗效及预后
▲ 建议对PAH患者病情严重程度进行评估,包括心功能、运动耐量、血清生化标记物、超声心动图及血流动力学指标等(Ⅰ,C)
▲ 病情稳定的PAH患者建议每3~6个月随访1次(Ⅰ,C)
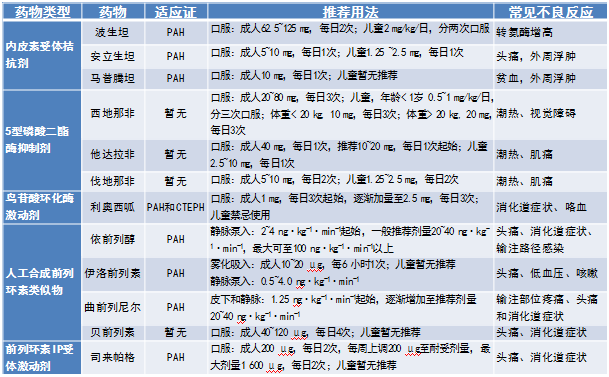
▲ 建议给予充分靶向药物治疗,使PAH患者病情达到或维持低危状态(Ⅰ,C)
▲ 若PAH患者经靶向药物治疗病情仍进展或维持中危状态,应考虑靶向药物治疗不充分(Ⅱa,C)
▲ 对接受药物治疗的PAH患者建议在专人指导下进行运动康复锻炼(Ⅱa,C)
▲ WHO心功能Ⅲ~Ⅳ级且动脉血氧分压<60mm Hg的PAH患者乘坐飞机时建议吸氧(Ⅱa,C)
▲ PAH患者进行择期手术建议尽可能选择硬膜外麻醉(Ⅱa,C)
▲ PAH患者运动锻炼时以不引起明显不适为宜(Ⅱb,C)
▲ 合并右心功能不全和液体潴留的PAH患者应给予利尿剂治疗(Ⅰ,C)
▲ IPAH、遗传性PAH及药物相关PAH可考虑长期口服抗凝剂治疗(Ⅱb,C)
▲ 合并矛盾性栓塞的艾森曼格综合征、合并肺动脉原位血栓形成的PAH患者需酌情抗凝治疗(Ⅱb,C)
▲ PAH患者应纠正贫血和/或缺铁状态(Ⅱb,C)
▲ PAH患者不建议使用ACEI、ARB、β受体阻滞剂及伊伐布雷定,除非合并相关疾病如高血压、冠心病或左心功能衰竭等(Ⅲ,C)
▲ IPAH、遗传性PAH及药物相关PAH患者如急性肺血管扩张试验阳性,给予大剂量钙通道阻滞剂治疗(Ⅰ,C)
▲ 建议对接受大剂量钙通道阻滞剂治疗的IPAH、遗传性PAH及药物相关PAH患者密切随访,治疗3~4个月后全面再评价(包括右心导管检查)(Ⅰ,C)
▲ 对WHO心功能Ⅰ~Ⅱ级且血流动力学明显改善甚至接近正常的IPAH、遗传性PAH及药物相关PAH患者,建议继续给予大剂量钙通道阻滞剂治疗(Ⅰ,C)
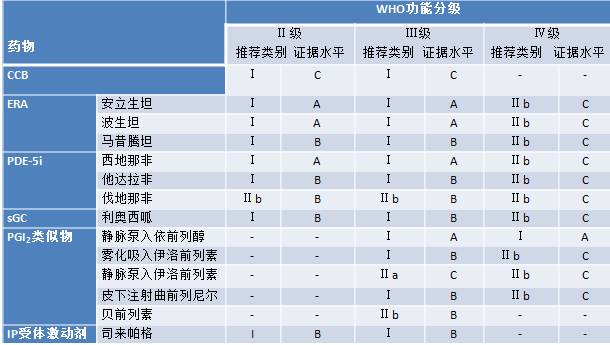
▲ 对WHO心功能Ⅲ~Ⅳ级或血流动力学改善不明显的PAH患者,建议启动PAH靶向药物治疗(Ⅰ,C)
▲ 对未接受急性肺血管扩张试验或结果阴性的患者,不建议应用大剂量钙通道阻滞剂治疗(Ⅲ,C)
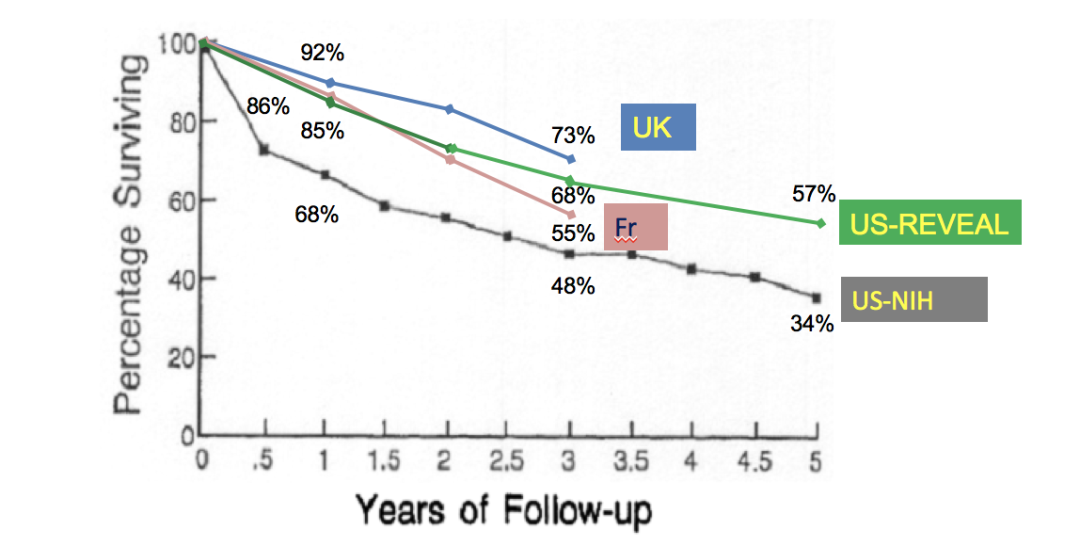
▲ PAH患者长期预后仍不理想
▲ 理论上联合治疗较单药治疗疗效更好
▲ 序贯联合和起始联合均可显著减少PAH患者临床恶化事件
▲ 危险分层为中危或高危的患者均推荐联合治疗,除PAH危险分层为低危的患者、老年患者和疑诊PVOD/PCH患者
▲ 我国PAH患者接受联合治疗的比例显著提升,但能接受起始充分联合治疗的比例仍非常低
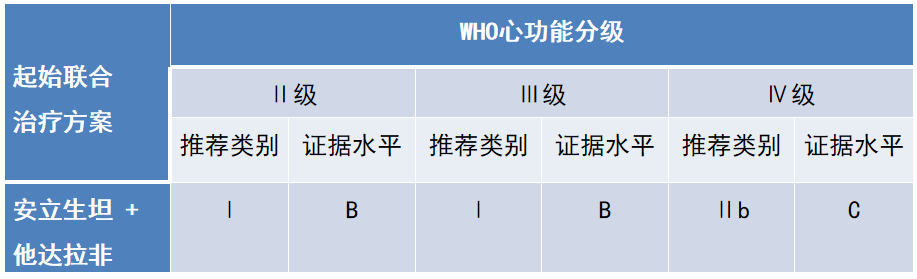
▲ 对WHO心功能Ⅳ级患者,建议先给予以静脉或皮下前列环素为基础的联合治疗至少3个月,仍然疗效不佳时可考虑肺移植或心肺联合移植
根据WHO心功能分级推荐转入重症监护、房间隔造口术及肺或心肺联合移植的建议
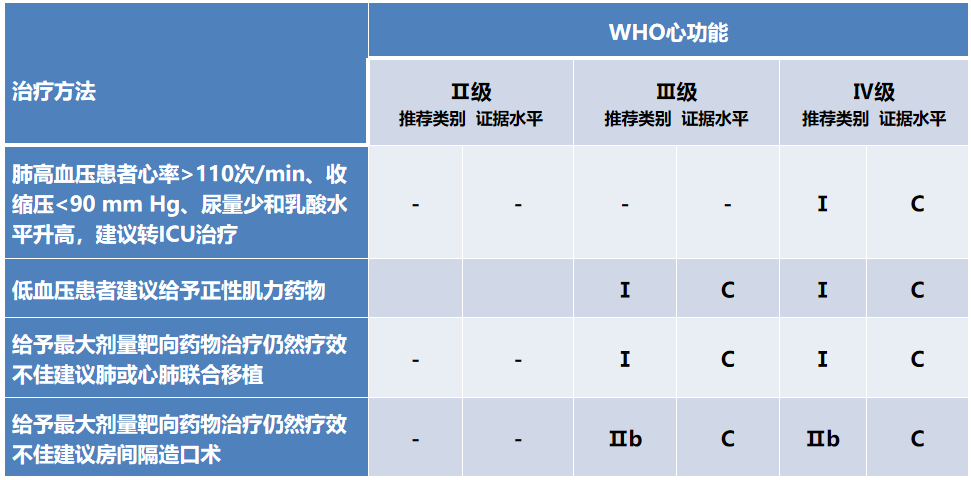
▲ CTEPH是未溶解的血栓发生机化导致肺血管床阻塞所致
▲ 这种纤维机化血栓可造成不同级别肺动脉分支的完全阻塞或不同程度的狭窄,并在血管腔内形成条索和分隔
▲ CTEPH不仅存在肺血管腔的机械性狭窄和梗阻,在非机化血栓梗阻区还存在与PAH类似的肺小动脉病变
▲ 急性PE病史:尤其复发性PE、大面积PE和特发性PE
▲ 血液学因素:遗传性易栓症、VIII因子、Von Willebrand因子水平升高、非O血型等
▲ 其他合并疾病:原发或继发性?、脾切除、脑室心房分流手术、起搏器感染、慢性炎性疾病(骨髓炎,炎症性肠病)、甲状腺功能低下及恶性肿瘤等
▲ 血栓栓塞:肺灌注扫描、CTPA或肺动脉造影显示一个或以上段级肺动脉充盈缺损
▲ 肺高血压:右心导管测量mPAP ≥ 25 mmHg,同时PAWP ≤ 15 mmHg
Irene. Eur Respir J 2013; 41: 462–468
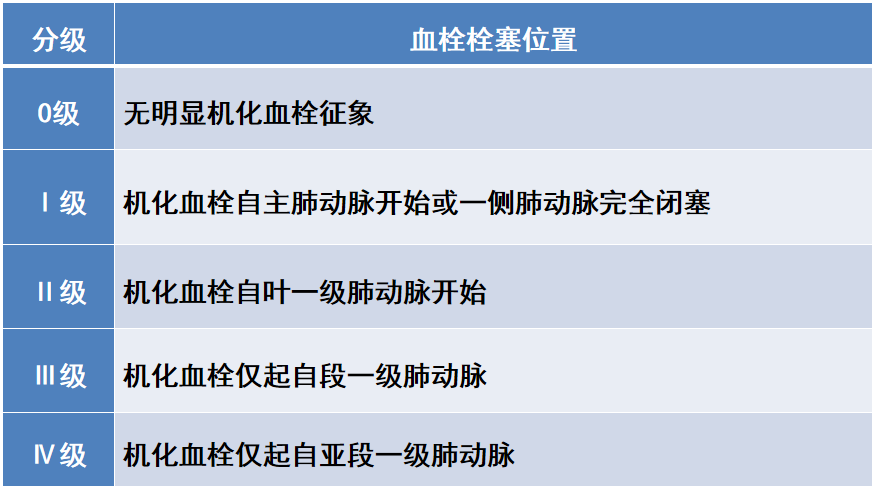
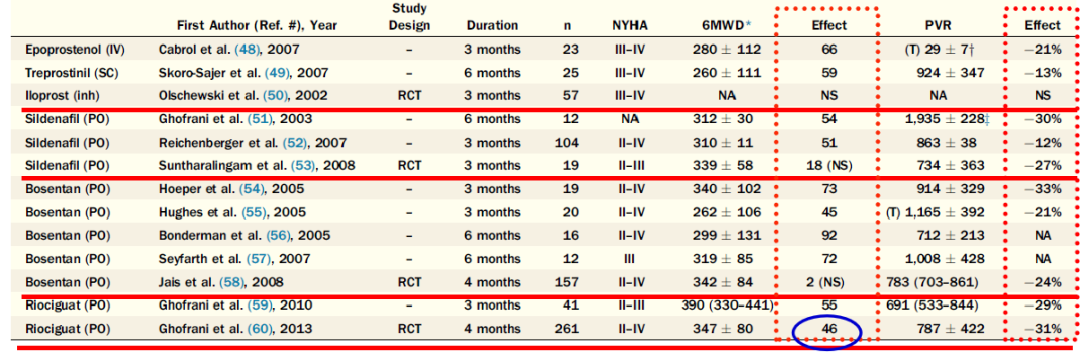
利奥西呱是迄今为止唯一具有CTEPH治疗适应证的药物
▲ 推荐对所有CTEPH患者首先进行肺动脉内膜剥脱术可能性评估
— 肺动脉阻塞部位:越靠近近端血管越容易剥离,目前手术可以剥离到段一级肺动脉水平
— 肺循环血流动力学状态:术前评价需考虑肺动脉阻塞面积和肺循环血流动力学参数是否匹配,肺血管阻力显著升高患者围术期死亡率也相应增加
— 合并症情况:有经验的中心肺动脉内膜剥脱围术期死亡率可低至2.2%~3.5%
▲ PEA术后5年生存率为82%,10年生存率可达75%
▲ 建议有条件开展肺动脉内膜剥脱术的中心积极开展此项工作
▲ 对不适合行肺动脉内膜剥脱术的CTEPH患者(Ⅲ/Ⅳ级病变为主、合并手术禁忌证、拒绝手术或术后残余肺高血压)可尝试行改良经皮肺动脉球囊扩张治疗
▲ 研究显示,逐步、多次经皮肺动脉球囊扩张治疗不但能显著改善CTEPH患者的血流动力学参数和症状,还能有效减少围术期并发症
▲ 改良经皮肺动脉球囊扩张治疗后5年生存率可达95%以上
▲ 术中最常见并发症为肺血管机械损伤所致的咯血或夹层,术后常见并发症为再灌注性肺水肿和对比剂肾病等
黄岚教授
陆军军医大学第二附属医院
中共党员,主任医师,军队专业技术二级教授,博士研究生导师,是我国心血管病防治领域杰出的专家之一。享受国家政府津贴和军队优秀人才岗位一类津贴,国家心血管病领域杰出专家,中华医学会心血管分会副主任委员、中国医师协会心血管分会副主任委员、中央军委保健委员会专家、重庆市医学会心血管病学专委会主任委员等学术任职。是我国“肺动脉栓塞诊治”“肺动脉高压诊治”“心力衰竭”“冠心病介入治疗”等指南的主要撰写人。先后获得国家科技进步二等奖1项、军队及省部级科技进步一等奖2项、医疗成果一等奖1项,二等奖3项、三等奖3项,发表论文276篇,其中SCI收录70余篇;培养研究生百余名。荣获“中国医师奖”、“白求恩式好医生”、“国之名医·卓越建树”“重庆市首席医学专家”等荣誉称号。